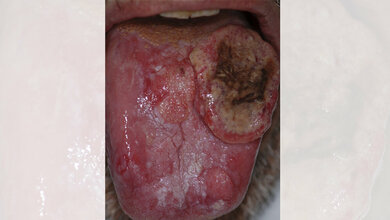
Tumore in der Nasenhöhle und der Nasennebenhöhle sind schwer zu diagnostizieren, da sie oft kein spezifisches Muster oder Erscheinungsbild aufweisen. Besonders gilt dies für die sogenannten sinonasalen undifferenzierten Karzinome oder kurz SNUCs. Sie beschränken sich zwar auf einen kleinen Raum, umfassen aber ein sehr breites Spektrum mit vielen Tumorarten. Nun ist es einem Team um Dr. Philipp Jurmeister und Prof. Frederick Klauschen vom Pathologischen Institut der LMU sowie Prof. David Capper von der Charité, zudem Wissenschaftler im Deutschen Konsortium für Translationale Krebsforschung (DKTK), Partnerstandorte München und Berlin, gelungen, die Diagnostik entscheidend zu verbessern: Sie entwickelten ein KI-Tool, das auf der Basis chemischer DNA-Modifikationen Tumore zuverlässig unterscheidet und die mit den bislang verfügbaren Methoden nicht unterscheidbaren SNUCs vier deutlich unterschiedlichen Gruppen zuordnet.
DNA-Methylierungsmuster erfasst
Chemische Modifikationen der DNA spielen bei der Regulation der Genaktivität eine entscheidende Rolle. Dazu gehört auch die DNA-Methylierung, bei der DNA-Bausteine mit einer zusätzlichen Methylgruppe versehen werden. Bereits in früheren Studien konnten die Wissenschaftlerinnen und Wissenschaftler zeigen, dass das Methylierungsmuster des Erbguts für verschiedene Tumorarten spezifisch ist, weil es auf die Ursprungszelle des Tumors zurückgeführt werden kann.
„Darauf basierend haben wir nun die DNA-Methylierungsmuster von fast 400 Tumoren in Nasen- und Nasennebenhöhle erfasst“, sagt Capper. Dank einer umfangreichen internationalen Kooperation gelang es den Forscherinnen und Forschern, eine so große Probenzahl zusammenzutragen, obwohl diese Tumore selten sind und insgesamt nur etwa vier Prozent aller bösartigen Tumoren im Hals-Nasen-Bereich ausmachen.
Einsatz eines KI-Modells
Für die Analyse der Methylierungsdaten entwickelten die Wissenschaftler und Wissenschaftlerinnen ein KI-Modell, das die Tumore verschiedenen Klassen zuordnet. „Methoden des maschinellen Lernens sind dabei aufgrund der großen Datenmenge unerlässlich“, betont Jurmeister. „Um tatsächlich Muster zu erkennen, mussten wir in unserer Studie mehrere Tausend Methylierungspositionen auswerten.“ Dabei zeigte sich, dass SNUCs in vier Gruppen eingeteilt werden können, die sich auch noch bezüglich weiterer molekularer Eigenschaften unterscheiden.
Gezielte neue Therapieansätze?
Diese Ergebnisse sind auch klinisch relevant, da die unterschiedlichen Gruppen verschiedene Prognosen haben. „Eine Gruppe beispielsweise verläuft überraschend gut, obwohl die Tumoren unter dem Mikroskop sehr aggressiv aussehen“, erläutert Klauschen. „Eine andere Gruppe dagegen hat eine schlechte Prognose.“ Auf der Basis der molekularen Eigenschaften der Gruppen könnten Forscherinnen und Forscher möglicherweise in Zukunft auch gezielte neue Therapieansätze entwickeln.
Quelle: idw/LMU
Artikel teilen