Die genetischen Eigenschaften der äußerst diversen Tumoren im Kopf- und Halsbereich sind bisher wenig untersucht. Auch geeignete Parameter zur Risikoeinschätzung innerhalb der Gruppe der Hochrisikopatientinnen und -patienten fehlten bislang. Vor diesem Hintergrund ist die aktuelle Studie zu sehen, die ein Forschungsteam um Lukas Kenner vom Klinischen Institut für Pathologie der MedUni Wien und Alexander Haug von der Universitätsklinik für Radiologie und Nuklearmedizin der MedUni Wien in Kooperation mit dem Christian Doppler Labor für Metabolomik und dessen Unternehmenspartner Siemens Healthineers durchgeführt hat. Dabei analysierten die Wissenschafter/-innen mittels DNA-Sequenzierung von 127 Gewebeproben erkrankter Patientinnen und Patienten sowie der Positronen-Emissions-Tomografie (PET) als bildgebendem Verfahren die zellulären Merkmale der Tumoren mittels Methoden der künstlichen Intelligenz (KI). Ziel der retrospektiven Studie war es, durch eine Zusammenführung der Daten von Gen-Analyse und Bildgebung spezifische Zahlen zu berechnen, die als Marker für die Risikoeinschätzung bei Patientinnen und Patienten eingesetzt werden können.
Gestörte genetische Netzwerke identifiziert
Zunächst erfolgte eine Sequenzierung der DNA aus den Gewebeschnitten sowie eine Auswertung der dreidimensionalen PET-Bilder von Patientinnen und Patienten, wobei spezifische Bildmuster extrahiert wurden. Durch die Zusammenführung des Datenmaterials auf Basis maschinellen Lernens gelang es dem Forschungsteam, in den Tumoren unterschiedlich gestörte genetische Netzwerke zu identifizieren, die eine zelluläre Seneszenz auslösen. Das bedeutet, dass sich Zellen nicht teilen und keine Entzündungsbotenstoffe ausschütten, aber nicht sterben. Problematisch dabei ist, dass solche Zellen Moleküle in benachbarte Gewebe ausschütten können, die zur Förderung der Tumorentwicklung beitragen.
Rasch gezieltere Therapien entwickeln
Das Ergebnis der Studie zeige, dass die vorgefundene zellulare Seneszenz gemeinsam mit den spezifischen, extrahierten Mustern mit einem hohen Risiko für Kopf-Hals-Krebspatienten verbunden sei, so die Forscher. Resümierend lasse sich feststellen, dass die rechnerisch identifizierten Marker aus genetischen und Bild-basierten Daten die Heterogenität der Tumoren besser abbilden können. So sei es möglich, rasch gezieltere Therapien zu entwickeln und anzuwenden sowie Hochrisikopatienten engmaschiger zu überwachen.
Hintergrund:
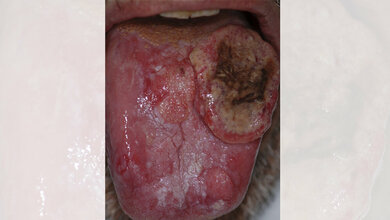
Unter dem Begriff Kopf-Hals-Tumoren werden verschiedene Krebsarten zusammengefasst, die in diesem Bereich auftreten. Dazu gehören Karzinome der Mundhöhle, des Rachens, des Kehlkopfes sowie der Nase und Nasennebenhöhlen. Bei den meisten malignen Tumoren handelt es sich um Plattenepithelkarzinome, also Tumoren, die von Oberflächenzellen ausgehen. Seltener sind Adenokarzinome, die dem drüsenartigen Gewebe entstammen und Sarkome aus Weichteilen. Weltweit werden Schätzungen der internationalen Datenbank Global Cancer Studies zufolge mehr als 830.000 Personen jährlich mit Kopfhalskrebs diagnostiziert. In Österreich erkrankten 2019 gemäß Statistik Austria 1.184 Männer und 404 Frauen an Krebs im HNO-Bereich. Risikofaktoren sind Rauchen und Alkoholkonsum, jedoch können auch Viren wie Humane Papillomaviren Krebs verursachen.
Quelle: MedUni Wien
Artikel teilen