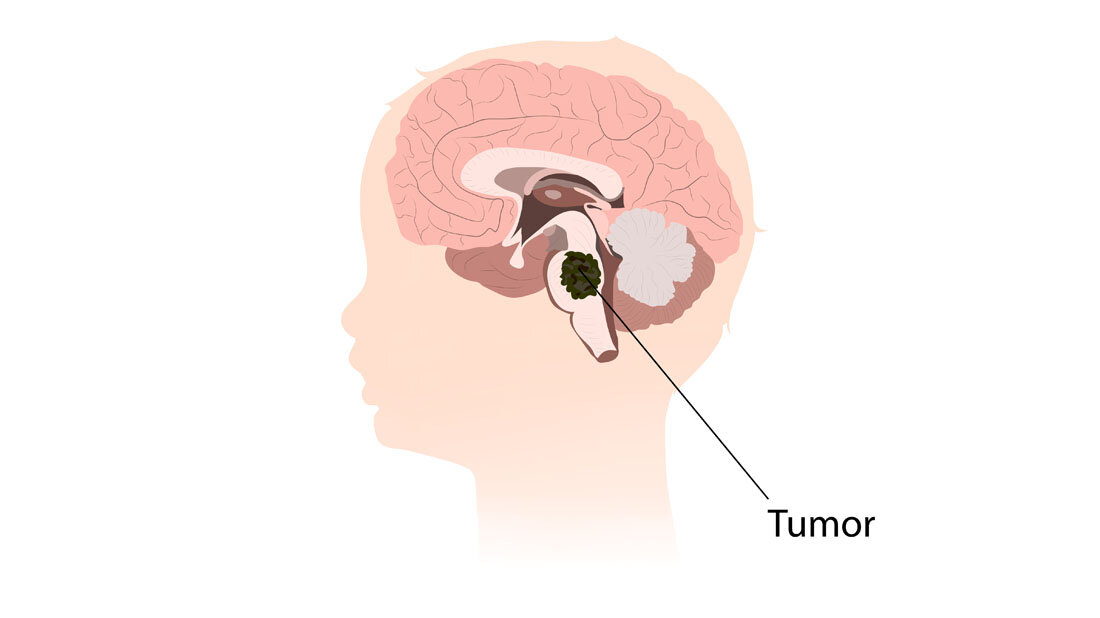
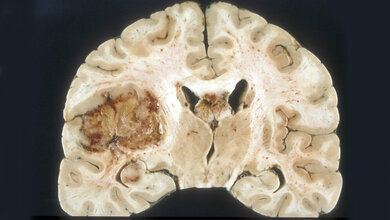
Diffuse Mittellinien-Gliome zählen zu den aggressivsten Hirntumoren. Sie treten meist bei Kindern und jungen Erwachsenen in der Nähe des Hirnstamms auf und sind daher operativ nur schwer zugänglich. Auch Chemo- oder Strahlentherapie sind nur begrenzt wirksam. Bei dieser Krebsart treten charakteristischerweise Mutationen im Gen für das Histon H3 (H3K27M) auf, einem Verpackungsprotein der DNA. Die Mutation lässt eine neuartige Proteinstruktur entstehen – ein so genanntes Neoepitop, das vom Immunsystem des Patienten als fremd erkannt werden kann.
Problem an der Wurzel packen
„Solche Mutationen, die in identischer Form bei vielen Patienten auftreten, sind selten bei Krebs. Sie bieten sich für die Entwicklung von Tumorimpfungen förmlich an, weil sie in allen Krebszellen auftreten, da das mutierte Histon ursächlich für die Entstehung der Mittellinien-Gliome ist. Das bedeutet, dass die Impfung gegen das mutierte Protein das Problem an der Wurzel packt“, erklärt Michael Platten, Direktor der Klinik für Neurologie der Universitätsmedizin Mannheim und Abteilungsleiter im Deutschen Krebsforschungszentrum (DKFZ).
Phase 1-Studie läuft noch
Entscheidend für den Erfolg von Krebsimpfungen sind Proteinstrukturen, an denen die Immunzellen den Krebs erkennen können – und die auf gesunden Zellen nicht (oder nur in geringem Maße) vorhanden sind. Mutationen im Tumorerbgut führen häufig zu krebstypisch veränderten Proteinstrukturen. Die Forscher um Katharina Sahm und Michael Platten bauten den Abschnitt des Histon H3-Proteins mit der charakteristischen Mutation synthetisch nach. Mit diesem Peptid konnten sie an einem Maus-Modell das Wachstum von H3K27M-mutierten Tumoren drosseln*. Ermutigt von den Ergebnissen entschied das Team, den an der Universität Tübingen hergestellten mutationsspezifischen Impfstoff in einer Phase1-Studie (INTERCEPT-H3), die noch nicht abgeschlossen ist, bei Patienten zu prüfen.
Auch individuelle Heilversuche mit dem Peptidimpfstoff
Parallel dazu behandelten die Ärztinnen und Ärzte gemeinsam mit Kollegen aus München, Berlin, Bonn und Münster acht erwachsene Patientinnen und Patienten im Rahmen zeitlich begrenzter individueller Heilversuche mit dem Peptidimpfstoff. Diese Patienten, die nicht in das Studienprotokoll aufgenommen werden konnten, litten an nach einer Standardtherapie fortschreitenden diffusen Mittellinien-Gliomen mit H3K27M-Mutation. Einige der Betroffenen erhielten neben der Tumorimpfung noch eine Therapie mit Immun-Checkpoint-Inhibitoren.
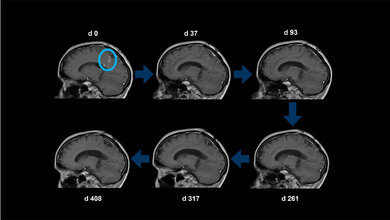
Bei keinem der Geimpften beobachteten die Ärztinnen und Ärzte schwerwiegende Nebenwirkungen. Fünf der acht behandelten Patienten entwickelten spezifische Immunantworten gegen das mutierte Protein, dabei stand die Aktivierung von CD4-T-Helferzellen im Vordergrund. Bei einer der Betroffenen, die eine starke Immunreaktion gezeigt hatte, bildete sich der Tumor komplett zurück, sie blieb für 31 Monate tumorfrei.
Wiederholte Gabe notwendig?
Das mit 27 Aminosäuren vergleichsweise lange Impfpeptid funktionierte bei Patienten mit verschiedenen HLA-Varianten. HLA-Proteine sind für die Präsentation des mutierten Peptids auf der Zelloberfläche zuständig und unterscheiden sich je nach genetischem Hintergrund von Mensch zu Mensch. Unterstützt durch das HI-TRON Mainz – Helmholtz-Institut des DKFZ beobachteten die Forscher außerdem, dass die Immunreaktionen mit der Zeit abnahmen, sodass eine wiederholte Gabe des Impfstoffs eine anhaltende Wirkung unterstützen könnte.
Auswertung der Studie voraussichtlich ab etwa 2025
„Darüber hinaus gehende Aussagen zur Wirksamkeit der Impfung können wir anhand dieser Behandlungen nicht machen. Auf jeden Fall hat uns die aktuelle Untersuchung wertvolle Hinweise gegeben, die uns helfen, die Entwicklung von Hirntumorimpfungen in Zukunft noch weiter zu optimieren“, erklärt die Letztautorin der Studie Katharina Sahm, Oberärztin der Neurologischen Universitätsklinik Mannheim und Mitarbeiterin des DKFZ. Derzeit läuft eine Phase 1-Studie, um den Impfstoff gegen die H3K27M-Mutation bei Patientinnen und Patienten mit neudiagnostizierten Mittellinien-Gliomen zu prüfen. Mit der Auswertung ist voraussichtlich ab etwa 2025 zu rechnen. Das Projekt wurde unter anderem aus Mitteln des Förderprogramms Translationale Onkologie der Deutschen Krebshilfe gefördert.
Quelle: DKFZ
Artikel teilen