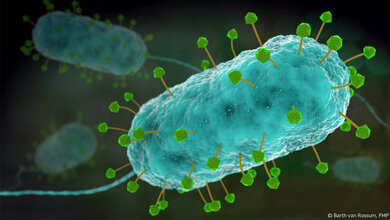
Um Bakteriophagen als Arzneimittel zuzulassen, haben sich das Fraunhofer-Institut für Toxikologie und Experimentelle Medizin ITEM, das Leibniz-Institut DSMZ-Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, die Charité – Universitätsmedizin Berlin und die Charité Research Organisation GmbH zum Forschungsverbund „Phage4Cure“ zusammengetan. Bakteriophagen erkennen hochspezifische Stämme einer bestimmten Bakterienart, befallen diese und zerstören sie schließlich. In Osteuropa werden sie bereits als Alternative zur traditionellen Antibiotikatherapie eingesetzt, in der Europäischen Union sind sie bisher jedoch noch nicht zugelassen. Die Gründe hierfür sind fehlende Qualitätsstandards in der Herstellung und ein Nachweis in systematisch klinischen Studien, dass die Therapie sicher, verträglich und wirksam ist.
Pseudomonas aeruginosa als Ziel
Das ist nun das Ziel der Projektpartner. Hauptaugenmerk liegt auf Bakteriophagen, die sich gegen das Bakterium Pseudomonas aeruginosa richten. Dieses Bakterium ist sehr häufig multiresistent und kann unter anderem eine Lungenentzündung auslösen. „Unser mittelfristiges Ziel ist es, Phagen als neuartige und zusätzliche Therapie für verschiedene Infektionskrankheiten und in unterschiedlichen Verabreichungsformen als Arzneimittel zu entwickeln – insbesondere da, wo Antibiotika gegenwärtig an ihre Grenzen gelangen", sagt Dr. Holger Ziehr, Projektkoordinator und Leiter der Pharmazeutischen Biotechnologie am Fraunhofer ITEM.
Die Partner des Forschungsverbundes bearbeiten je nach Expertise unterschiedliche Aspekte dieses Projekts. Am Leibniz-Institut DSMZ sollen gegen Pseudomonas aeruginosa gerichtete Bakteriophagen identifiziert und genetisch charakterisiert werden. Hier gilt es, Phagen zu finden, die einen Großteil der Pseudomonas-aeruginosa-Stämme erkennen. Sind diese identifiziert, werden sie zur weiteren Hochaufreinigung und pharmakologischen Herstellung an das Fraunhofer ITEM übergeben. Dort wird ein sogenannter plattformartiger Herstellungsprozess für Phagen-Wirkstoffe entwickelt. Somit ist der Herstellungsprozess auch auf andere Phagen übertragbar. Außerdem werden dort bereits präklinische Prüfungen durchgeführt.
Die weiteren präklinischen Prüfungen werden an der Charité – Universitätsmedizin Berlin durchgeführt, wo auch die Konzeptionierung, Planung und Durchführung der klinischen Prüfung unter anderem stattfinden wird. Auf der Forschungsstation der Charité Research Organisation GmbH (CRO) wird letztendlich die klinische Studie durchgeführt. Außerdem wird die CRO das Gesamtprojekt organisatorisch und regulatorisch begleiten, engen Kontakt zu den Arzneimittelbehörden pflegen sowie das Datenmanagement, die Statistik und die Erstellung des klinischen Studienreports übernehmen.
Quelle: Pressemitteilung des Fraunhofer ITEM
Artikel teilen