Reparierende Fähigkeiten von Klebsiella pneumoniae
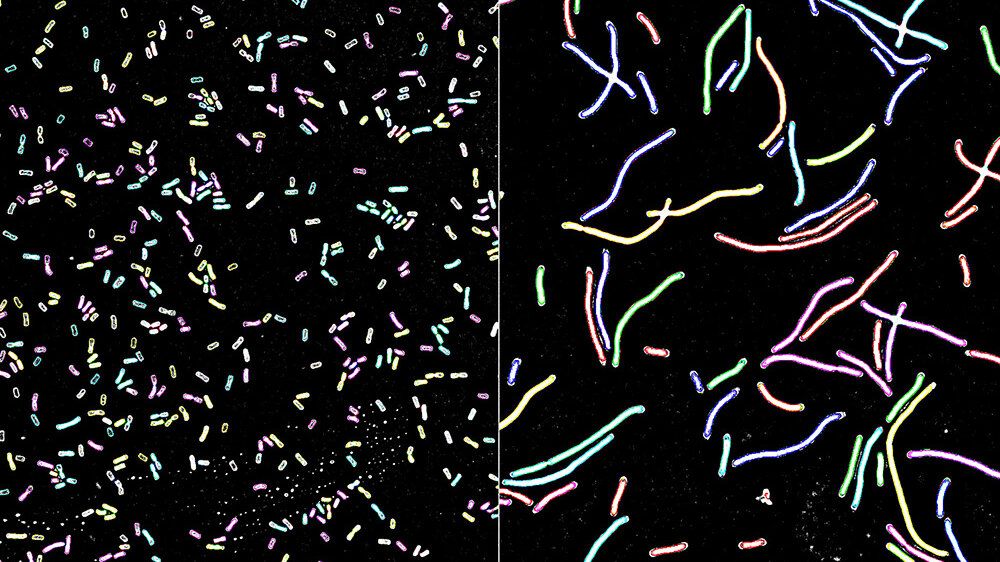
Klebsiella pneumoniae sorgt unter anderem für Entzündungen des Magen-Darm-Traktes, Lungenentzündungen, Wundinfektionen oder sogar Blutvergiftungen. Da das Bakterium sehr anpassungsfähig ist, ist es besonders interessant und relevant in der Klinik. Es vermehrt sich nicht nur schnell, sondern ist auch in der Lage, neben den natürlichen Resistenzen gegen antibiotische Wirkstoffe weitere zu erwerben. Zudem ist gegenüber verwandten Spezies wie E. coli wenig über die Genregulation in K. pneumoniae bekannt.
Ein Forschungsteam des Exzellenzclusters Balance of the Microverse der Universität Jena um Dr. Kathrin Fröhlich untersuchte das Transkriptom nach bisher unbekannten sRNAs und auf Hinweise anderer Funktionen. „Dabei haben wir neben vielen sRNAs, die bereits aus verwandten Bakterien bekannt waren auch über 50 neue potenzielle Regulatoren gefunden“, erläutert Eric Ruhland, Erstautor und Doktorand am Jenaer Exzellenzcluster.
Unterbrechung der Zellteilung
Zu den sRNAs ermittelte das Team auch die dazugehörigen Interaktionspartner, wobei die sRNA DinR den Forschenden ins Auge fiel. „Wir konnten schließlich herausfinden, dass DinR von der Zelle produziert wird, wenn DNA-Schäden auftreten. Unter dieser Bedingung hemmt DinR die Bildung von FtsZ, einem für die Zellteilung wichtigen Strukturprotein“, erklärt Ruhland. Falls Defekte im Erbgut vorhanden sind, kann Klebsiella mittels DinR die Zellteilung stoppen –ein bisher unbekannter Mechanismus des Bakteriums. So erhält die Zelle Zeit, die DNA zu reparieren und sichert möglichst gesunde Generationen ohne DNA-Schäden.
Doch die Reparatur sei fehleranfällig und es komme zu einer gehäuften Mutationsrate so Fröhlich. Dies kann wiederum zu neuen Antibiotikaresistenzen führen oder die Widerstandsfähigkeit der Bakterien maßgeblich verändern. „Wir möchten zukünftig verstehen, wie genau Klebsiella mit der DNA-Schädigung umgeht, und welche Rolle sRNAs für die vergleichsweise hohe Anpassungsfähigkeit der Bakterienspezies spielen, durch die Klebsiella vor allem im klinischen Bereich immer problematischer wird“, führt Fröhlich fort. „Mit dieser Studie tragen wir zu einem besseren Verständnis für die grundlegenden molekularbiologischen Prozesse in Klebsiella bei, aus dem sich auch Wege eröffnen können, Infektionen gezielter zu behandeln.“
Quelle: idw
Artikel teilen




