Bis zur 41. Kalenderwoche hat das Robert Koch-Institut für Deutschland schon 3.530 Fälle erfasst. Zum gleichen Zeitraum des Vorjahres waren es erst 3.283. Dies entspricht einer Zunahme um 7,5 Prozent im laufenden Jahr. Eigentlich sollte die Tuberkulose laut WHO in den Niedriginzidenzländern bis 2035 auf weniger als 1 pro 100.000 Einwohner gesenkt werden. Doch davon ist selbst Deutschland noch weit entfernt. Die globalen Auswirkungen auf die Epidemiologie der Tuberkulose durch bewaffnete Konflikte, Flucht und Migration betreffen auch die eigentlichen Niedriginzidenzländer. Hinzu kommen die Probleme mit resistenten Erregern, die auch durch die häufigen Therapieabbrüche verursacht werden.
Neue Therapien gegen Tuberkulose?
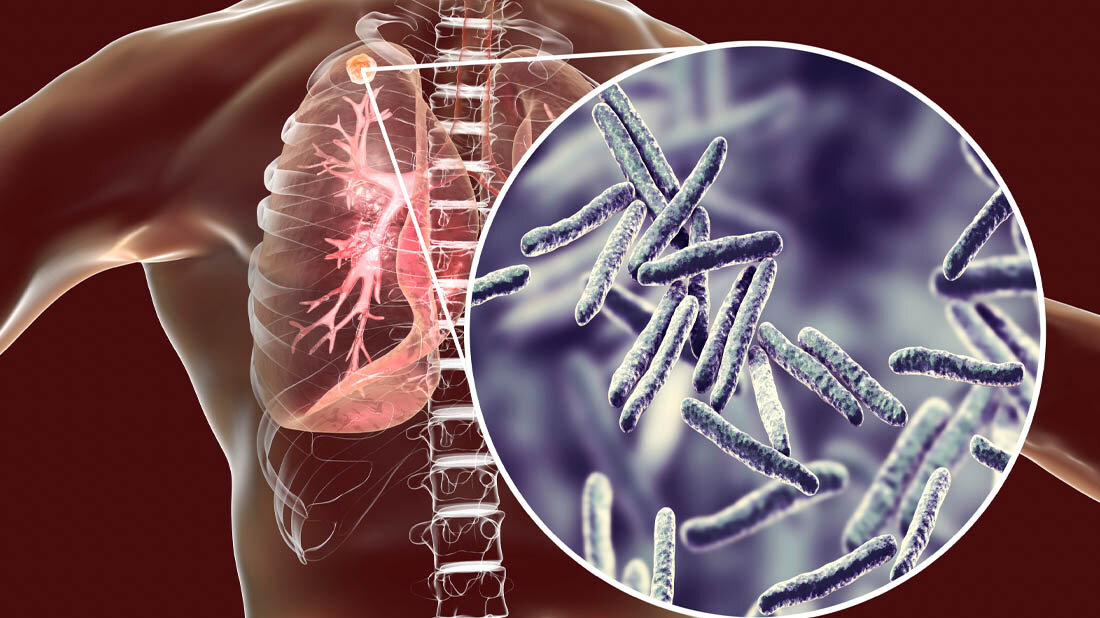
Ein Forscherteam der Ecole Polytechnique Federal de Lausanne unter der Leitung von Dr. Vivek Thacker, jetzt Gruppenleiter am Zentrum für Infektiologie des Universitätsklinikums Heidelberg, hat nun untersucht, warum sich Tuberkulosebakterien zu langen Strängen aneinanderlagern und wie dies ihre Infektionsfähigkeit beeinflusst. Ihre Erkenntnisse könnten zu neuen Therapien führen. Der Ausgang einer Infektion mit Mycobacterium tuberculosis reicht von Abwehr ohne jedwede Erkrankung bis hin zu chronischer Infektion mit Auszehrung und Tod. Diese große Variabilität ist wesentlich von der Immunabwehr des infizierten Wirts abhängig. Die Analyse des Erreger-Wirt Wechselspiels ist zentrales Forschungsthema der Abteilung Medizinische Mikrobiologie und Hygiene im Zentrum für Infektiologie im Universitätsklinikum Heidelberg (UKHD) und an der Medizinischen Fakultät Heidelberg (MFHD).
Bedeutung der Stränge von Mycobacterium tuberculosis
Lange bekannt ist, dass Mycobacterium tuberculosis den Cordfaktor ausbildet, der für die krankmachenden Eigenschaften des Erregers, seine Virulenz, wichtig ist, und der außerdem zu einem besonderen Wachstumsverhalten führt: Mycobacterium tuberculosis kann dichtgepackte Stränge aus vielen Bakterien produzieren, die sich lichtmikroskopisch beobachten lassen. Wie diese Stränge zu den krankmachenden Eigenschaften von Mycobacterium tuberculosis beitragen, war bislang im Wesentlichen unverstanden.
Wissenschaftler und Wissenschaftlerinnen um Dr. Vivek Thacker, bis vor kurzem tätig an der EPFL in Lausanne und nun Gruppenleiter im Zentrum für Infektiologie des Universitätsklinikums Heidelberg, haben in der aktuellen Arbeit erstmals einen Zusammenhang zwischen diesem „mechanischen“ Wachstumsverhalten und der Infektionsbiologie von Mycobacterium tuberculosis hergestellt. In einem interdisziplinären Forschungsansatz nutzten sie Lebendzellmikroskopie und synthetische Organmodelle („lung-on-chip“).
Unempfindlich gegen die Wirkung von Antibiotika
„Wir konnten zeigen, dass die Kompression von Bakterien zur Speicherung von Energie über den Cordfaktor in der Membran des Erregers führt“, berichtet Thacker. „Dadurch können Erreger, die von Fresszellen in der Lunge aufgenommen wurden und eigentlich vernichtet werden sollten, auch innerhalb dieser Abwehrzellen strangförmig wachsen.“ Das Team um Thacker beobachtete, dass dieses Wachstum den Zellkern der Wirtszelle einschnürt und stranguliert. Dadurch kann die Zelle weniger Abwehr- und Botenstoffe bilden und deshalb den Erreger nicht eindämmen. Weiterhin führt das strangförmige Wachstumsverhalten außerhalb von Zellen dazu, dass sich der Erreger zwischen den Epithelzellen, welche die Lungenbläschen auskleiden, und in andere Organe des Körpers ausbreiten kann. Schließlich konnte das Forscherteam beobachten, dass Bakterien in solchen Strängen unempfindlich gegen die Wirkung von Antibiotika werden und nach Beendigung einer Antibiotikatherapie erneut wachsen können.
Mechanopathologie wird für Therapiesuche wichtiger
„Es ist uns gelungen, mechanisches Wachstumsverhalten auf zellulärer Ebene mit biologischen Funktionen zu verknüpfen“, sagt Thacker. „Diese Mechanopathologie ist ein neues, vielversprechendes Forschungsfeld.“ Einige Aspekte dieses mechanischen Wachstumsverhaltens erinnern an Biofilme, die andere wichtige Erreger von Infektionskrankheiten, z. B. Staphylokokken und Pseudomonaden, ausbilden und die ebenso zur Unempfindlichkeit gegen Antibiotika und Hemmung der Wirtsabwehr beitragen. Die Verknüpfung von physikalischem Wachstumsverhalten und Infektionsbiologie ist damit ein höchst interessantes Forschungsgebiet, welches neue Erkenntnisse für die Entwicklung von dringend benötigten Therapien schaffen könnte.
Quelle: idw/Uniklinikum Heidelberg
Artikel teilen