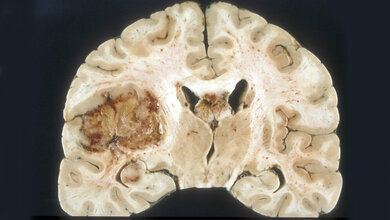
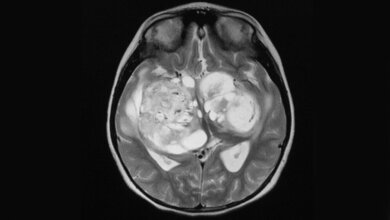
Rund 8.000 Menschen erkranken in Deutschland jährlich neu an Hirntumoren. Diese Tumoren machen damit etwa zwei Prozent aller Krebserkrankungen aus. Unter den hirneigenen Tumoren sind die von den Stützzellen des Gehirns ausgehenden Gliome mit sechs Erkrankungen pro 100.000 Einwohner und Jahr am häufigsten. Bei ungefähr der Hälfte dieser Patienten wird dabei ein Glioblastom, das heißt die bösartige Ausprägung einer Hirntumorerkrankung, festgestellt.
Vollständige Entfernung oft nicht möglich
„Bösartige Gliome wie das Glioblastom haben die Eigenschaft, diffus in das angrenzende Gehirngewebe einzuwachsen. Dadurch ist eine vollständige chirurgische Entfernung sämtlicher Tumorzellen meist nicht möglich“, erklärt Prof. Dr. med. Guido Reifenberger vom Institut für Neuropathologie der Heinrich Heine Universität in Düsseldorf. „Im Anschluss an die Operation ist daher eine Strahlen- und Chemotherapie notwendig, um die verbliebenen Tumorzellen zu bekämpfen. Allerdings können auch dadurch meist nicht alle Tumorzellen abgetötet werden und der Tumor entwickelt sich erneut, das heißt es kommt zu einem Tumorrezidiv.“
Molekulare Biomarker verbessern die Diagnostik von Hirntumoren
Hoffnung geben neue molekularpathologische Verfahren, mit denen Hirntumoren viel genauer diagnostiziert und individuell für Patienten gezielte Therapieansätze identifiziert werden können. Große Fortschritte wurden in den letzten Jahren durch neue Erkenntnisse zu den molekularen Veränderungen erzielt, die für die Entstehung und das Wachstum von verschiedenen Hirntumorarten verantwortlich sind. Unterschiedliche Hirntumoren zeigen dabei verschiedene Modifikationen. Diese können im Tumorgewebe durch neuartige molekularpathologische Methoden bestimmt werden und als sogenannte Biomarker die Diagnosestellung erheblich verbessern. Außerdem können sie das Ansprechen auf bestimmte therapeutische Wirkstoffe vorhersagen und somit zu einer gezielteren Behandlung des einzelnen Patienten genutzt werden.
Wesentliche Bedeutung für die Klassifikation
„Die molekulare Diagnostik hat inzwischen eine wesentliche Bedeutung bei der Klassifikation von Hirntumoren erlangt. Einer der zentralen Tests für Gliome bezieht sich auf den Nachweis von Mutationen in den Genen Isozitratdehydrogenase 1 und 2. Hierdurch werden biologisch und prognostisch unterschiedliche Arten von Gliomen zuverlässig unterschieden“, betont Prof. Reifenberger. „Bei der Bildung von Hirntumoren kommt es durch mutierte Proteine zu zahlreichen Veränderungen in den Zellprozessen, die das Zellwachstum fördern oder die gegen den Tumor gerichtete Immunabwehr hemmen. Die molekulare Diagnostik liefert ein breites Spektrum an Informationen, über die wir unterschiedliche Hirntumoren genauer voneinander abgrenzen können. Je nach Mutation können dann gegebenenfalls gezielt Medikamente eingesetzt und eben auch präzisere Vorhersagen über die Entwicklung des Tumors gemacht werden.“
MGMT-Test zur Vorhersage
Die molekularen Verfahren erlauben zudem Aussagen, wie einzelne Tumoren auf Strahlen- oder Chemotherapie ansprechen. In der Regel erhalten Patienten mit einem Glioblastom eine Kombination beider Therapieformen. Insbesondere bei älteren Patienten ist diese Kombination aber manchmal zu belastend. Hier kann dann ein bestimmter Biomarker, der sogenannte MGMT-Test, vorhersagen, ob bei dem Patienten eher eine Strahlentherapie oder eine Chemotherapie wirksam ist.
Neue Methoden der Hochdurchsatz-Sequenzierung
Eine weitere vielversprechende Entwicklung ist die Hochdurchsatz-Sequenzierung. Bei diesem neuen Verfahren werden nicht nur einzelne Gene auf charakteristische Merkmale getestet, sondern in einem Experiment lässt sich gleichzeitig eine Vielzahl von Genen unter die „Lupe“ nehmen.
Krebserkrankungen entstehen dadurch, dass sich die Abfolge der Grundbausteine der Erbsubstanz in den Tumorzellen verändert, also Mutationen auftreten. Das führt dann zum unkontrollierten Zellwachstum und zur Tumorentstehung. „Mit der Hochdurchsatz-Sequenzierung, englisch "Next Generation Sequencing", lassen sich heute in wenigen Tagen alle wichtigen Mutationen in einem Tumor nachweisen. Das Muster an Veränderungen erlaubt dann wiederum eine umfassendere molekulare Klassifikation sowie eine Vorhersage, ob der Tumor für eine bestimmte, molekular zielgerichtete Therapie geeignet ist“, so Prof. Reifenberger. Die Zukunft der Tumordiagnostik gehört der Hochdurchsatz-Sequenzierung, davon ist Prof. Reifenberger überzeugt: „Die Forschung liefert ständig neue Ergebnisse. Immer mehr klinisch relevante Tumor-Gene werden gefunden. Diese können in Zukunft nicht mehr in einer Einzelgen-Analyse, sondern nur durch parallele Analyse multipler Gene untersucht werden.“
Integrierte Diagnostik erstmals in WHO-Klassifikation festgeschrieben
Mit der seit Mitte 2016 international geltenden, von der Weltgesundheitsorganisation (WHO) herausgegebenen WHO-Klassifikation der Tumoren des zentralen Nervensystems wurde für die Diagnostik von Hirntumoren zum ersten Mal der Nachweis verschiedener Biomarker verpflichtend festgeschrieben. Vorher erfolgte die Befundung ausschließlich auf der Basis von histologischen Diagnosen, also der Beurteilung von gefärbten Schnittpräparaten des Tumorgewebes unter dem Mikroskop.
Wesentlich präzisere Diagnosestellung
„Wir profitieren heute davon, dass gemäß der neuen WHO-Klassifikation bei der Diagnose eines Hirntumors Erkenntnisse aus drei Ebenen zusammen fließen“, so die Einschätzung des Düsseldorfer Neuropathologen. „Wir haben erstens die Ergebnisse der klassischen histologischen Untersuchung, zweitens die Parameter zur Beurteilung des Tumors gemäß der WHO-Gradierung und drittens die Ergebnisse der molekularen Tests. Daraus ergibt sich dann eine ‚integrierte Diagnose‘, die in der Praxis zu einer wesentlich präziseren Diagnosestellung führt und damit die beste Behandlung für den einzelnen Patienten sicherstellt.“
Neueste Forschungsergebnisse zum Thema werden auf dem diesjährigen Kongress der Deutschen Gesellschaft für Neuropathologie und Neuroanatomie e.V. (DGNN) präsentiert. Dieser findet gemeinsam mit der Jahrestagung der Deutschen Gesellschaft für Pathologie e.V. (DGP) vom 22. bis 24. Juni 2017 in Erlangen statt. Weitere Informationen unter www.pathologie-dgp.de. (idw, red)
Artikel teilen