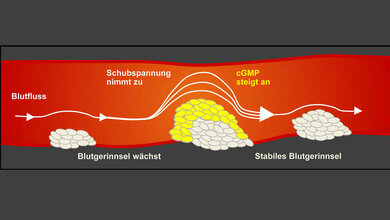
Bei einem Herzinfarkt ist Eile geboten. Weil das Herzgewebe nicht ausreichend durchblutet wird, beginnt es abzusterben. Eine Komplikation sind laut DZHK Herzrhythmusstörungen, die sich zu einem lebensbedrohlichen Kammerflimmern entwickeln und in einem plötzlichen Herztod enden können. 40 Prozent der Betroffenen sterben innerhalb des ersten Tages, fast die Hälfte davon an einem plötzlichen Herztod. Erfolgt bereits kurz nach dem Ereignis eine Revaskularisation, wird also das verschlossene Gefäß wieder geöffnet, kann ein Infarkt allerdings fast folgenlos ausheilen. Vergehen jedoch mehr als 24 Stunden, ist das Gewebe nicht mehr zu retten und der Körper beginnt mit der „Aufräumarbeit“. Fresszellen des Immunsystems räumen tote Zellen ab, was mit heftigen Entzündungen verbunden ist. Schließlich wandern Bindegewebszellen ein und bilden Narbengewebe.
Pumpfunktion global stark eingeschränkt
Die überschießende Entzündung und Narbenbildung kann dabei auch die Randbereiche des Infarkts betreffen und sogar auf weiter entfernte Regionen des Herzens übergreifen. „Diese Menschen entwickeln oft eine besonders schwere Form der ischämischen Herzschwäche. Die Herzkammer ist dann ballonartig aufgebläht und die Pumpfunktion global stark eingeschränkt“, sagt Prof. Philip Wenzel vom DZHK-Standort Rhein-Main im Zentrum für Kardiologie der Universitätsmedizin Mainz. Er und sein Team am dortigen Centrum für Thrombose und Hämostase sind der Frage nachgegangen, was dabei eigentlich passiert und ob sich dieser überschießende bindegewebige Umbau des Herzens verhindern lässt.
Weniger Herzschwäche im Mausmodell
Die Wissenschaftler untersuchten Herzgewebe von Patientinnen und Patienten, die infolge eines Infarktes eine langanhaltende ischämische Herzschwäche entwickelt hatten und fanden vermehrt Proteine, die an Gerinnungs- und Fibroseprozessen beteiligt sind, wie sie auch bei einem akuten Infarkt vorkommen. Als Vergleich diente ihnen Gewebe von gesunden Spendern, beispielsweise aus Organen, die nicht transplantiert werden konnten.
Sie fanden heraus, dass an der Signalübertragung der Entzündungsprozesse auch bestimmte Entzündungszellen, die Monozyten beteiligt sind. Wenn die Forscher auf den Monozyten die Signalübertragung des Gerinnungsfaktors Tissue Factor und seines Rezeptors PAR2 blockierten, bildete sich weniger Wachstumsfaktor TGF-ß1 und in Folge weniger überschießende Fibrose. Dies führte im Mausmodell zu weniger Herzschwäche, besserer Herzleistung und weniger Sterblichkeit.
NaPC2 als Wirkstoffkandidat
Auch ein lang bekanntes, gerinnungshemmendes Medikament namensNaPC2 kann den neu gefundenen Signalweg hemmen und wäre damit aus Sicht von Wenzel ein Wirkstoffkandidat, mit dem sich die chronische ischämische Herzschwäche behandeln oder sogar verhindern ließe. „Bei den Mäusen haben wir einen eindeutigen Effekt auf die Pumpleistung gesehen, diese war dank des Medikaments nur halb so stark eingeschränkt.“ Ließe sich das auf den Menschen übertragen, wäre das der Unterschied, ob ein Herzinfarkt-Opfer mit verzögerter Wiederdurchblutung eine schwere Herzschwäche entwickelt und kleinste Anstrengungen nicht mehr bewältigen kann. Oder ob der Betroffene in der Lage wäre, voll ins Leben zurückzukehren und seinen Alltag selbständig zu verrichten, so Wenzel.
Möglicher Biomarker im Blick
„Wir haben festgestellt, dass Patientinnen und Patienten mit subakutem Herzinfarkt, also verzögerter Behandlung nach Beschwerdebeginn, eine pathologische Aktivierung des pro-fibrotischen Signalwegs schon in den zirkulierenden Monozyten in der Blutbahn aufweisen. Hier haben wir möglicherweise einen Biomarker an der Hand, der uns helfen könnte, Personen mit erhöhtem Risiko für die Entwicklung einer schweren Herzschwäche nach Infarkt zu identifizieren“. Die Forscher wollen die Signalwege weiter im Detail untersuchen und herausfinden, welche Patienten besonders von einer Therapie profitieren würden.
Quelle: idw/DZHK
Artikel teilen