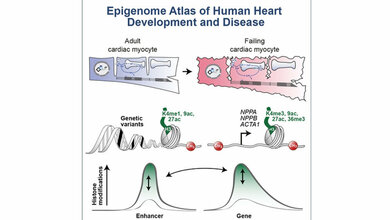
Immer wieder wird auch über Herzprobleme nach einer COVID-19-Erkrankung berichtet. Etwa jeder Dritte klagt nach einer schweren COVID-19-Erkrankung über Beschwerden und Funktionseinschränkungen des Herzens. Schwere Krankheitsverläufe einer COVID-19-Infektion beeinträchtigen nicht nur die Lungenfunktion, sondern können auch lebensbedrohliche Folgen für das Herz hervorrufen. Das Spektrum reicht dabei von einer akuten Herzmuskelentzündung (Myokarditis) bis zu einer chronischen Einschränkung der Pumpfunktion des Herzens. Die grundlegenden Schädigungsmuster konnten bis zum heutigen Tag nicht gänzlich nachgewiesen werden. Ein interdisziplinäres Forschungsteam um Professor Dr. Danny Jonigk, Christopher Werlein und Privatdozent (PD) Dr. Mark Kühnel vom Institut für Pathologie der Medizinischen Hochschule Hannover (MHH) hat jetzt mit Hilfe innovativer molekularer Verfahren und eines hochauflösenden Mikroskopieverfahrens gezeigt, wie die andauernde Entzündung bei COVID-19 das Herzgewebe angreift und langfristig die kleinsten Herzkranzgefäße umbaut, indem spezielle Vorläuferzellen des Immunsystems aus dem Blut in das Herz gelotst werden.
Fehlaktivierte Entzündungszellen
Um die Mechanismen dieser langanhaltenden Herzmuskelschädigung aufzuklären, haben die Forscherinnen und Forscher Herzgewebe von Patientinnen und Patienten mit schweren COVID-19-Verläufen untersucht und diese mit Gewebeproben nach schweren Grippe-Infektionen durch das Influenzavirus sowie nach schweren, durch andere Viren verursachte Herzmuskelentzündungen verglichen. Obwohl bei der COVID-19-Herzschädigung – anders als bei den Vergleichsproben – äußerlich keine klassische Entzündung des Herzgewebes festzustellen war, fand das Forschungsteam jedoch eine große Ansammlung von fehlaktivierten Entzündungszellen: sogenannte Makrophagen und ihre Vorläuferzellen, die Monozyten. „Diese Monozyten haben eine herausragende Bedeutung als Vorläuferzellen der Blutgefäßneubildung und können in kürzester Zeit das Blutgefäßsystem umbauen“, erklärt Christopher Werlein, Erstautor der Studie.
COVID-19 kann alle Gefäße im Körper angreifen
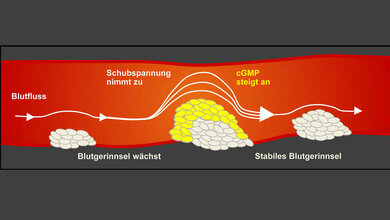
Ausgelöst durch die Infektion mit dem Coronavirus SARS-CoV-2 sammeln sich in den nur wenige Millimeter dicken Herzgefäßen kleinste Verstopfungen an. „Diese Ultrathromben verändern den Blutstrom erheblich und damit auch die Sauerstoffversorgung“, betont PD Dr. Kühnel. Das ruft die Monozyten auf den Plan, die sich an die inneren Gefäßwände heften und dort neue Verzweigungen ausbilden. Diesen Gefäßumbau – in der Fachsprache intussuszeptive Angiogenese genannt – hat das Team bereits zuvor in anderen Organen von COVID-19-Betroffenen als charakteristisches Schädigungsmuster beschrieben. Was möglicherweise als kurzfristige Rettungsreaktion des Körpers gedacht ist, um den verminderten Blutfluss und die Unterversorgung mit Sauerstoff auszugleichen, könnte zur chronischen Schädigung des Herzens und zu Long COVID führen, vermuten die Forscher. „Auf jeden Fall bestätigen die neuesten Untersuchungen unsere frühere Annahme, dass SARS-CoV-2 systemisch alle Gefäße im Körper angreift und diese langfristig umbaut“, betont Professor Jonigk.
Die Arbeit ist in Kooperation mit dem Deutschen Zentrum für Lungenforschung (DZL) am Standort Hannover BREATH, der Universitätsklinik Aachen, der Universitätsmedizin Mainz und der Georg-August-Universität Göttingen entstanden.
Quelle: idw/MHH
Artikel teilen