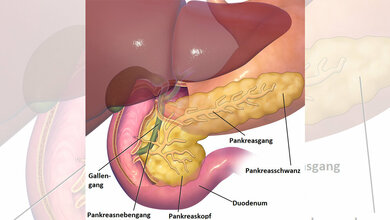
Das Pankreas (die Bauchspeicheldrüse) ist eines der größten Drüsen des menschlichen Körpers. Sie produziert Verdauungsenzyme und Hormone. Jedes Jahr erkranken nach Angaben des Robert Koch-Instituts ca. 19.000 Menschen an einem Pankreas-Karzinom. Die jährlichen Sterbefälle sind praktisch genauso hoch. Die relative 10-Jahres-Überlebensrate beträgt demnach nur 7 bis 8%, somit zählt das Pankreas-Karzinom zur vierthäufigsten Todesursache unter allen Krebsarten. Neue Therapiemethoden sind deshalb dringend notwendig.
Bisher kein Durchbruch in der Therapie
Besonders das metastasierte Pankreas-Karzinom wird als nicht heilbar angesehen. Eine schnelle Diagnostik und ein schneller Therapiebeginn sind hier äußerst wichtig. Nach der operativen Entfernung des Tumors erhalten Patienten eine adjuvante Chemotherapie, um noch im Körper befindliche Tumorzellen zu vernichten. Dennoch entwickelt das Pankreas-Karzinom häufig eine Resistenz gegenüber der Behandlung. Daneben gibt es auch zielgerichtete, personalisierte Therapieverfahren, die wichtige Signalwege des Tumors beeinflussen. Trotz der unterschiedlichen Therapiemethoden gab es innerhalb der letzten 30 Jahre keinen signifikanten Durchbruch bei der Therapie des Pankreas-Karzinoms. Die Arbeitsgruppen von Prof. Dr. Silke Härteis (Lehrstuhl für Molekulare und Zelluläre Anatomie, Univ. Regensburg), Prof. Dr. Thiha Aung (Lehrstuhl für Molekulare und Zelluläre Anatomie, Univ. Regensburg; Technische Hochschule Deggendorf), Prof. Dr. Christoph Brochhausen-Delius (ehemals Institut für Pathologie der UR, jetzt Direktor des Pathologischen Instituts am Universitätsklinikum Mannheim) und Prof. Dr. Christina Hackl (Klinik und Poliklinik für Chirurgie, Universitätsklinikum Regensburg) widmen sich deshalb diesem wichtigen Thema in einem Forschungsprojekt, das im Rahmen des Förderprogramms „Zentrales Innovationsprogramm Mittelstand“ des Bundesministeriums für Wirtschaft und Energie (BMWi; Projektform FuE-Kooperationsprojekte; AiF Projekt GmbH) mit einer ¾ Million Euro gefördert wird.
Entwicklung einer Drug-Screening-Plattform
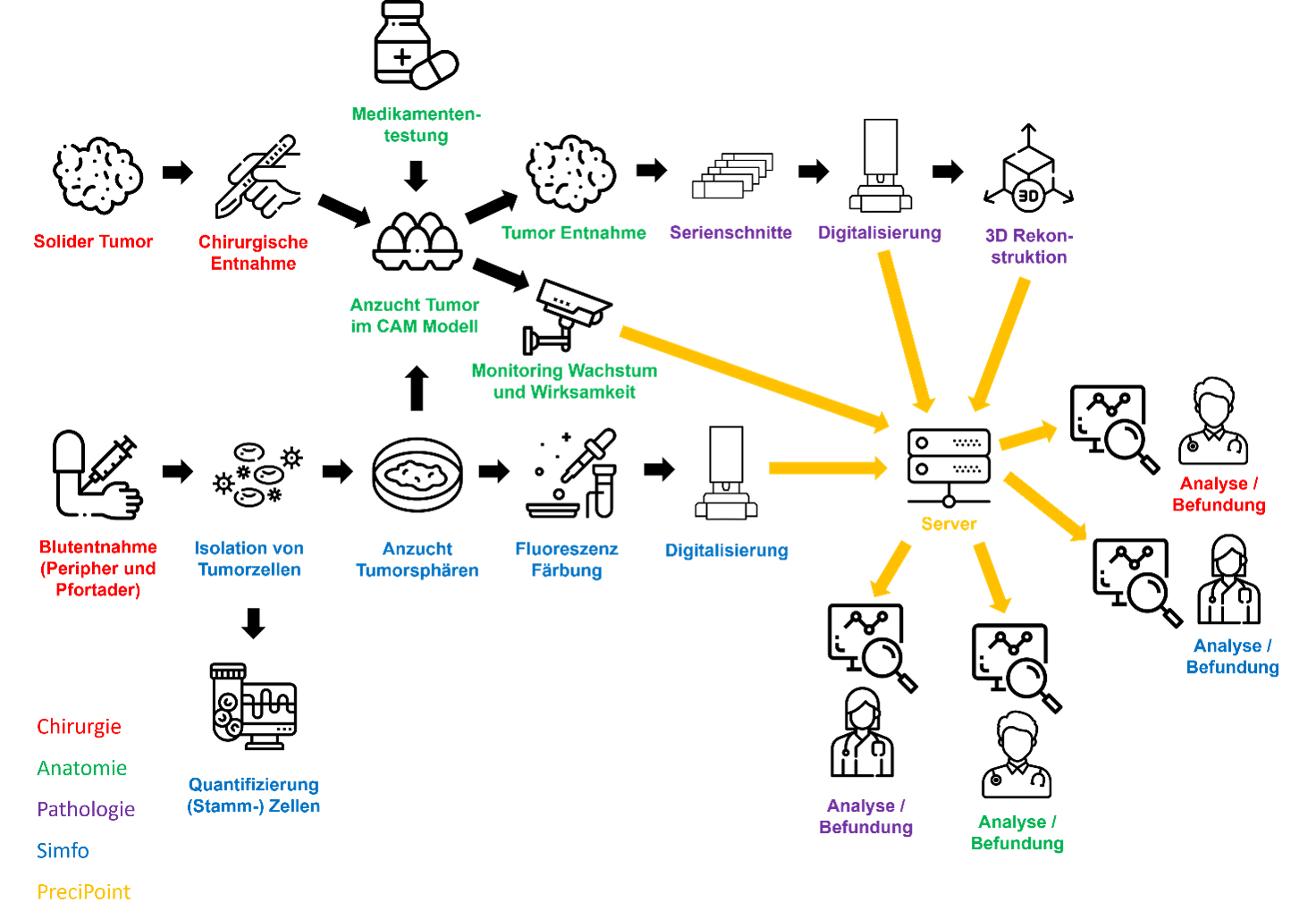
In dem Projekt soll ein neuartiges Screening-Tool entwickelt werden: eine Drug-Screening-Plattform. Damit soll es zu jedem Behandlungszeitraum möglich sein, die Wirkung der Therapeutika auf die Tumore zu ermitteln, um anschließend die bestmögliche Therapie durchführen zu können. Hierfür haben sich die Wissenschaftlerinnen und Wissenschaftler aus Universität und Klinikum mit weiteren Kooperationspartnern aus Klinik und Industrie zusammengeschlossen, um verschiedene innovative Methoden zu kombinieren.
Wichtige Patientengewinnung
Zur Gewinnung der Proben für das Projekt, werden am Universitätsklinikum Regensburg Patienten und Patientinnen bei der Aufklärung über die geplante Behandlung und über die Möglichkeit an der Studie teilzunehmen informiert. Christina Hackl koordiniert den studien-bezogenen Ablauf innerhalb der chirurgischen Abteilung. Stimmt ein Patient der Teilnahme zu, können Blut- und Tumorproben, die nicht für diagnostische Zwecke benötigt werden, sofort im Anschluss an die präoperative bzw. operative Entnahme zum Projektpartner gebracht werden.
Tumorsphären wachsen lassen
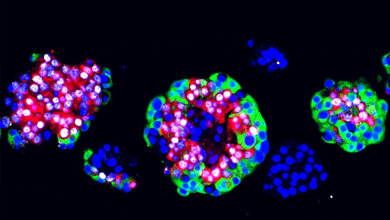
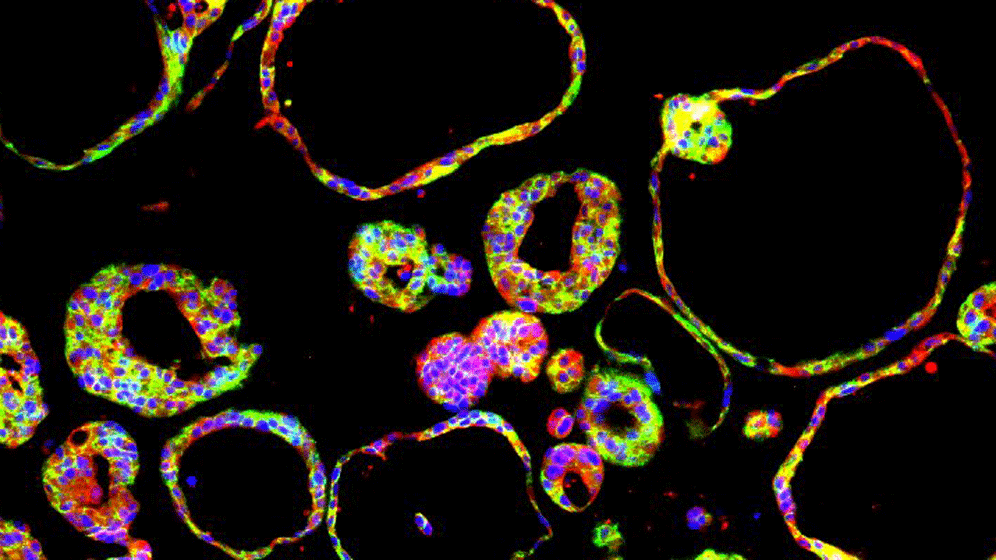
Aus dem Blut von Patientinnen und Patienten soll beim Projektpartner simfo GmbH aus Bayreuth die Subpopulation der Tumorzellen isoliert werden, um aus den Zellen sogenannte Tumorsphären (kugelartig Zellkolonien) wachsen zu lassen. Die Firma simfo GmbH besitzt bereits eine jahrelange Erfahrung in der morphologischen, molekularbiologischen und funktionellen Charakterisierung von ins Blut abgegebenen Zellen aus soliden epithelialen Tumoren. In der Arbeitsgruppe von Prof. Dr. Härteis und Prof. Dr. Aung werden die erhaltenen Tumorsphären und das Primärmaterial des Pankreastumors dann mittels Chorion-Allantois-Membran-Modell (CAM-Modell) kultiviert. Die Tumorsphären und das Tumorgewebe werden als sogenannte „patient-derived xenografts“ (PDX) auf der CAM Membran gezüchtet, welche die Tumorzellen und das Tumorgewebe wie eine Plazenta ernähren.
Tumorwachstum jederzeit bewerten
Durch den Versuchsaufbau könne das Tumorwachstum zu jeder Zeit bewertet werden. So könnten die Wirksamkeit und Selektivität von etablierten und auch neuen Therapeutika auf das Wachstum der Tumorzellen sowie auf Angiogeneseprozesse (Bildung neuer Blutgefäße) und das Einwachsen des Tumors in das umliegende Gewebe direkt analysiert werden. Auch Resistenzen auf Therapeutika könnten auf diesem Weg erkannt werden. Die exakte Charakterisierung des Tumorgewebes und der Tumorzellen finde zu einem Teil im Institut für Pathologie in der Arbeitsgruppe von Prof. Dr. Brochhausen-Delius durch strukturelle und ultrastrukturelle Analysen statt.
Erstellung von Schnittpräparaten
Dort sollen mit den Tumorsphären und dem Tumorgewebe histologische, immunhistologische und elektronenmikroskopische Untersuchungen durchgeführt werden. Dafür sollen mit den unterschiedlichen Proben aus dem CAM Modell Schnittpräparate erstellt werden. Die Proben sollen anschließend mit dem M8 Mikroskop (PreciPoint GmbH) gescannt werden, um Übersichtsaufnahmen der Schnittpräparate, sogenannte „Whole Slide Images“ (WSI), für die Analysen herzustellen. Mithilfe von Serienschnitten könne zudem eine 3-D-Rekonstruktion der immunhistologisch angefärbten Blutgefäße durchgeführt werden, um das Gefäßsystem und dessen Verzweigungen genauer darzustellen. Durch die Analysen könnten schließlich Aussagen über funktionale Moleküle, Wachstum des Tumors und der Blutgefäße getroffen werden, um so ein tieferes Verständnis über die Blutversorgung des Tumors und seines Aufbaus, auch im Vergleich zu metastasierten Tumoren, zu erhalten, so die Erwartungen.
Kontinuierliche Nachsorge der Patientinnen und Patienten
Ein weiterer Teil der histologischen und molekularbiologischen Analysen soll im Labor von Prof. Dr. Hackl stattfinden. Dort soll auch eine quantitative Auswertung der Proliferationsfähigkeit, Angioinvasion, Gewebeinvasion und dem Ansprechen auf die Chemotherapie durchgeführt werden. Parallel dazu erfolge durch Prof. Hackl die kontinuierliche Nachsorge der Patientinnen und Patienten im Rahmen der chirurgisch-onkologischen Sprechstunde sowie die Korrelation des klinischen Verlaufs mit den durch das Projekt erhobenen Tumorcharakteristika.
Virtuelle Vernetzung der Chirurgie, Labormedizin & Co.
Der Industriepartner PreciPoint GmbH aus Freising werde eine Online-Plattform schaffen und ermögliche dadurch die virtuelle Vernetzung der Chirurgie, Labormedizin, Anatomie, Pathologie und der Grundlagenforschung. Mithilfe der Plattform sollen die Metadaten, Befunddaten und Bilddaten direkt geteilt werden und die unterschiedlichen Abteilungen dadurch schnell und effektiv zusammenarbeiten können. Mit der Entwicklung neuer Algorithmen sollen strukturelle Analysen der Daten und das Wirkstoffscreening der Proben mit bestimmten Charakteristika ermöglicht werden. Eine weitere Neuerung werde eine Kombination aus Hellfeld- und fluoreszenzbasierter Mikroskopie sein, um die Darstellung der Bilder und die Ansicht zwischen unterschiedlichen Aufnahmemodi zu erleichtern.
Ziel der Drug-Screening-Plattform sei es schließlich, innerhalb eines für den betroffenen Patienten sehr kurzen Zeitraums die beste Therapieoption mit den geringsten Nebenwirkungen zu ermitteln, um die Behandlung von Pankreas-Karzinomen und letztlich auch weiteren Tumoren in Zukunft zu verbessern, so die Hoffnung der Forscherinnen und Forscher.
Quelle: idw/Uni Regensburg
Artikel teilen