Ein interdisziplinäreres Team der Molekular-Neurologischen Abteilung (Leiter: Prof. Dr. Jürgen Winkler) und der Stammzellbiologischen Abteilung (Leiterin: Prof. Dr. Beate Winner) des Uniklinikums Erlangen der Friedrich-Alexander-Universität Erlangen-Nürnberg (FAU) kam nun der Wirkweise einer Therapie auf die Spur, die derzeit klinisch erprobt wird. Die Forscherinnen und Forscher entdeckten, dass ein „small molecule“ den Abbau eines spezifischen, für die Eiweißsynthese notwendigen Botenmoleküls so beschleunigt, dass der Huntingtin-Spiegel bei Patientinnen und Patienten deutlich sinkt.
Ziel: RNA-modifizierende Ansätze
Ein small molecule ist eine organische Substanz mit einem niedrigen Molekulargewicht, das in der Lage ist, biologische Prozesse wie die Eiweißsynthese zu verändern. Mit dieser Studie konnte das interdisziplinäre Erlanger Team erstmals zeigen, wie Nervenzellen von Huntington-Patientinnen und -Patienten geheilt werden können. Die Ergebnisse sollen dazu beitragen, langfristig RNA-modifizierende Ansätze für tödlich verlaufende Erkrankungen wie Huntington in der klinischen Praxis umzusetzen und so Betroffene zu behandeln.
Verklumpungen in den Nervenzellen
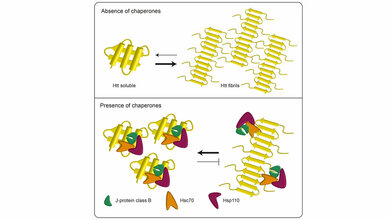
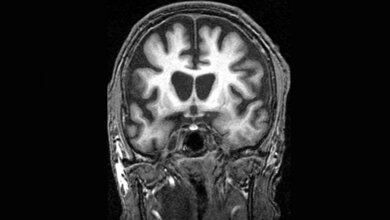
Die Erkrankung Chorea Huntington zeichnet sich durch zunehmende, nicht kontrollierbare, teils „einschießende“ Bewegungen aus („Veitstanz“). Neben dieser Bewegungsunruhe leiden Betroffene an schweren kognitiven Beeinträchtigungen und psychiatrischen Symptomen. Die meisten erkranken in jungem Alter, etwa 20 Jahre nach dem Ausbruch endet die Huntington-Erkrankung dann tödlich. Grund dafür ist eine spezifische Veränderung im Huntingtin-Gen, die mit einer Wahrscheinlichkeit von 50 Prozent vererbt wird. Genetisch kommt es zu wiederholten Verlängerungen eines kleinen Abschnitts im Huntingtin-Gen, zu sogenannten CAG-Repeats. Diese verursachen eine Verklumpung von Huntingtin in den Nervenzellen, was sie unwiderruflich zerstört.
Frühe klinische Phase-2a-Studie
Therapieansätze, die aktuell klinisch erprobt werden, versuchen, den Huntingtin-Spiegel zu senken. Diesen Ansatz untersuchen auch Forscherinnen und Forscher aus der Bewegungsambulanz der Molekularen Neurologie des Uniklinikums Erlangen im Rahmen einer sehr frühen klinischen Phase-2a-Studie. Dabei werden small molecules, im Fall der Erlanger Forscher der Wirkstoff Branaplam, als Tablette verabreicht; sie verringern den Huntingtin-Spiegel. Diese Erkenntnis führte zu einer ersten internationalen Studie des Pharmaunternehmens Novartis, die die Wirksamkeit von Branaplam bei der Huntington-Erkrankung überprüft.
Wirkmechanismus war unbekannt
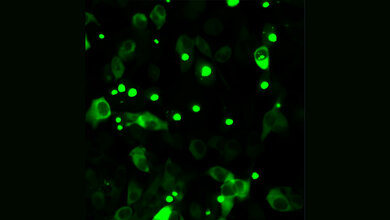
Um diese in menschlichen Nervenzellen von Huntington-Patientinnen und -Patienten aufzudecken, schloss sich ein interdisziplinäres Team aus den Bereichen Neurologie, Neurowissenschaft und Bioinformatik der Molekularen Neurologie und der Stammzellbiologie des Uniklinikums Erlangen zusammen. Mittels induzierter pluripotenter Stammzellen, die aus Hautzellen von Menschen gewonnen und anschließend in ein frühes Zellentwicklungsstadium versetzt werden, wurden im Labor Gehirnnervenzellen hergestellt. Das Team behandelte diese Nervenzellen von Huntington-Betroffenen mit Branaplam und entdeckte, dass sich das schädliche Huntingtin bereits nach Zugabe geringster Wirkstoffmengen verringerte.
Effekt auf das Spleißen von RNA-Biomolekülen
Im Vorfeld war bereits bekannt, dass Branaplam sich an RNA-Botenmoleküle bindet. Um aufzuklären, welche Effekte der Wirkstoff auf die RNA-Botenmoleküle hat, wurde die Gesamtheit aller RNA-Moleküle in vielen Zellreihen mittels RNA-Sequenzierung gemessen. Dr. Florian Krach aus der Erlanger Stammzellbiologie gelang es mittels biostatistischer Verfahren und auf Basis künstlicher Intelligenz, den Wirkmechanismus in dieser enormen Datenmenge zu entschlüsseln: Demnach hat Branaplam einen bedeutenden Effekt auf das sogenannte Spleißen von RNA-Biomolekülen. Dabei werden nicht benötige Abschnitte der RNA-Botenmoleküle entfernt. Dies wird ebenfalls beim RNA-Botenmolekül des Huntingtin-Gens beobachtet. Der nicht herausgeschnittene Abschnitt in der Huntingtin-RNA führt dazu, dass das RNA-Botenmolekül instabil und infolgedessen abgebaut wird – somit kann das genetisch veränderte Huntingtin gar nicht erst entstehen.
Quelle: idw/FAU
Artikel teilen