Die Beta-Zellen innerhalb der Langerhans-Inseln in der Bauchspeicheldrüse stellen das für den Zuckerstoffwechsel essentielle Hormon Insulin her. Insulin regt Körperzellen dazu an, Glukose aus dem Blut aufzunehmen und zu verstoffwechseln. Sterben die Beta-Zellen ab, kann der Körper den Zucker Glukose nicht mehr effizient genug verarbeiten, wodurch die Zuckerkonzentration im Blut steigt. Der betroffene Mensch erkrankt dadurch an Diabetes mellitus Typ II, einer potenziell lebensbedrohlichen Erkrankung, da ein zu hoher Blutzuckerspiegel die menschlichen Organe schädigt.
Auch Amylin wird gebildet
Zusammen mit Insulin wird in den Langerhans-Inseln das Peptidhormon Amylin gebildet und ausgeschüttet. Unter noch nicht genau bekannten Bedingungen können sich einzelne Amylin-Moleküle zu Amyloid-Aggregaten verbinden, welche sich in den Langerhans-Inseln ablagern und zum Absterben der Beta-Zellen führen. Die Düsseldorfer und Jülicher Forscher um Dr. Wolfgang Hoyer vom Institut für Physikalische Biologie der Heinrich-Heine-Universität und der Abteilung Strukturbiochemie (ICS-6) des Forschungszentrums Jülich haben ein neuartiges Bindeprotein, genannt Beta-Wrapin „HI18“, entwickelt, welches schon bei sehr geringen Konzentrationen die Amyloid-Aggregation stark hemmt. Dieses Bindemolekül kann damit ein Ansatz sein, um möglicherweise den Ausbruch von Diabetes mellitus Typ II bei Risikopatienten zu verhindern.
3-dimensionale Struktur untersucht
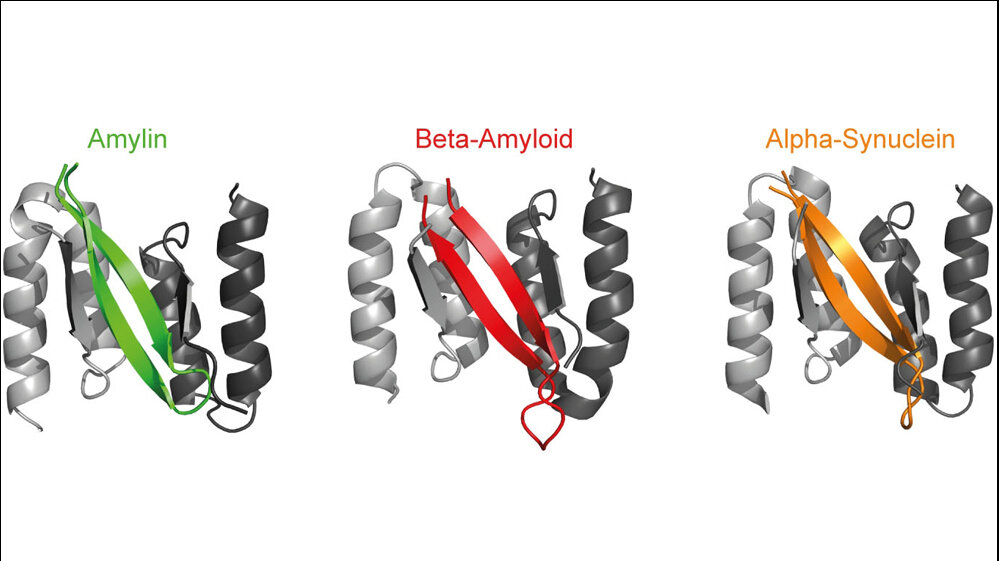
Die Forscher haben mithilfe der Kernspinresonanz-Spektroskopie die drei-dimensionale Struktur des an das Beta-Wrapin gebundenen Amylins in atomarer Auflösung untersucht. Sie fanden, dass Amylin dabei in einer so genannten Beta-Haarnadel-Struktur vorliegt, wie man sie ebenfalls in den Proteinen Beta-Amyloid und Alpha-Synuclein findet. Aggregate aus dem Beta-Amyloid-Protein gelten als verantwortlich für die Entstehung der Alzheimer-Demenz, während Alpha-Synuclein-Aggregate als ursächlich verantwortlich für die Parkinson-Erkrankung angesehen werden.
„Möglicherweise können die von uns entwickelten Beta-Wrapine nicht nur gegen die Diabetes-Entstehung wirken, sondern auch der Alzheimer-Demenz und der Parkinson-Krankheit vorbeugen oder deren Fortschreiten verzögern oder sogar aufhalten“, so Dr. Hoyer, der die Studie koordinierte. (idw, red)
E. A. Mirecka, S. Feuerstein, L. Gremer, G. F. Schröder, M. Stoldt, D. Willbold & W. Hoyer: β-Hairpin of Islet Amyloid Polypeptide Bound to an Aggregation Inhibitor. Scientific Reports, 6:33474. September 2016, DOI: 10.1038/srep33474
Artikel teilen