Um eine Krebserkrankung mit neuen, so genannten zielgerichteten Medikamenten zu behandeln, muss der Arzt zunächst eine Probe des Tumors analysieren. Dazu entnimmt er eine Gewebeprobe (Biopsie) und analysiert das Erbgut. Anhand der darin nachgewiesenen Mutationen wählt der Arzt die passende Therapie.
Gewebebiopsie empfindlich genug?
Die konventionelle Biopsie gilt zwar derzeit als der Goldstandard, doch ihre Möglichkeiten sind nicht unbegrenzt. Molekulare Anomalien und Mutationen in Tumoren verändern sich im Verlauf der Zeit und unter der Behandlung. Diese Erkenntnis warf die Frage auf, ob die Gewebebiopsie als Methode empfindlich genug ist, um solche dynamischen Veränderungen zu erfassen. „Außerdem ist die konventionelle Biopsie ein viel invasiveres und mitunter auch riskantes Verfahren“, erklärt Professor Holger Sültmann, Leiter der Arbeitsgruppe Krebsgenomforschung am DKFZ.
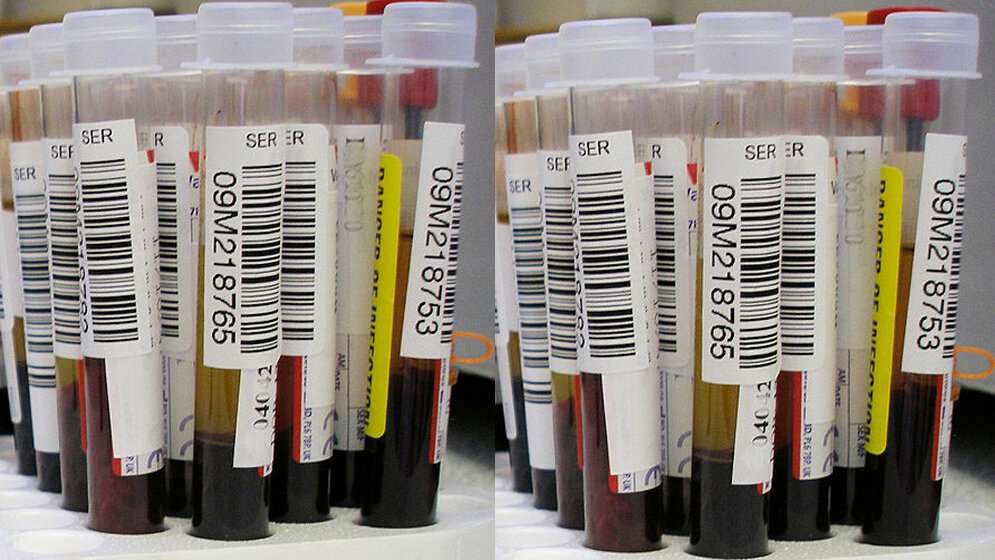
Seit einigen Jahren setzen Mediziner deshalb Hoffnung in die sogenannte Liquid Biopsy (flüssige Biopsie). Wenn Zellen absterben, gelangt ihre DNA ins Blut. Man spricht dann von „zellfreier DNA“, kurz cfDNA. Die cfDNA von Tumorzellen, die nach der Therapie absterben, weist Mutationen auf, die sich aus einer Blutprobe mittels PCR und nachfolgender Sequenzierung nachweisen lassen. „Im Unterschied zur Gewebeprobe werden bei der Liquid Biopsy lediglich ein paar Milliliter Blut entnommen; daraus wird die DNA isoliert und molekular analysiert“, erläutert Sültmann die Vorteile der neuen Methode.
Liquid Biopsy genauso sensitiv und zuverlässig?
Ob die Liquid Biopsy genauso sensitiv und zuverlässig wie eine Gewebeprobe ist und die gewonnenen klinischen Informationen ebenso aussagekräftig sind, wollte die Forschergruppe nun herausfinden. In Zusammenarbeit mit Kollegen von der Thoraxklinik Heidelberg untersuchten die Wissenschaftler vom DKFZ 16 Lungenkrebspatienten, deren Tumoren alle bestimmte Mutationen aufwiesen und die mit einem Tyrosinkinasehemmer (TKI) behandelt wurden. Bis zu zwei Jahre lang sammelten die Wissenschaftler von jedem Patienten regelmäßig Blutplasmaproben, aus denen sie anschließend die DNA isolierten. Mit digitalen PCR-Tests suchten sie nach mutierter cfDNA und verglichen die Zahl der nachgewiesenen Mutationen mit den klinischen Daten der Patienten zu den verschiedenen Zeitpunkten.
„Wir wollten testen, ob es überhaupt möglich ist, Mutationsveränderungen im (Blut-)Plasma im zeitlichen Verlauf zu identifizieren, und ob wir diese mit klinischen Parametern in Beziehung setzen können“, so Holger Sültmann. Die Datenanalyse erbrachte drei interessante Beobachtungen.
Drei interessante Beobachtungen
Erstens veränderte sich die Zahl der Mutationen bei den Patienten übereinstimmend mit dem klinischen Verlauf der Erkrankung. So zeigte sich bei einem Patienten gleich zu Beginn der TKI-Therapie ein drastischer und unmittelbarer (innerhalb der ersten 26 Stunden) Anstieg der Menge mutierter cfDNA im Blutplasma, was auf eine Vielzahl abgestorbener Krebszellen hindeutet und damit auf ein gutes Therapieansprechen. Interessanterweise fiel dieser Spitzenwert kurz darauf wieder ab, was vermuten lässt, dass die TKI-Therapie in den ersten Behandlungstagen ihre größte Wirkung hat. „Das zeigt, dass wir zum Therapiebeginn besonders genau überwachen müssen“, bemerkte Sültmann.
Zweitens beobachteten die Wissenschaftler, dass wenig oder gar keine cfDNA im Blutplasma nachzuweisen war, wenn die Krankheit längere Zeit unter Kontrolle war und der Tumor nicht wuchs.
Und schließlich zeigte sich bei Patienten, deren Tumor zurückgekehrt war und die kurz darauf verstarben, in kurzen Zeitabschnitten ein rascher Anstieg der cfDNA-Konzentration. Teilweise war dieser Anstieg sogar schon vor dem Auftreten klinischer Anzeichen zu beobachten.
Molekulare Daten können wichtige Informationen liefern
Diese Ergebnisse zeigen, dass die Liquid Biopsy sensitiv genug ist, um Tumorveränderungen in Echtzeit nachzuweisen. Dabei hat sie gleichzeitig den Vorteil, dass sie weniger invasiv als eine Gewebeentnahme ist. Die so gewonnenen molekularen Daten könnten den Klinikern auch Informationen liefern, die es erlauben, frühzeitig über geeignete therapeutische Strategien zu entscheiden. Da die Studie jedoch erst an 16 Patienten erfolgt ist, weist Holger Sültmann darauf hin, dass es noch zu früh für eine generelle Beurteilung der Liquid Biopsy ist: „Dies ist zunächst ein ‚Proof of Concept‘, mit der wir zeigen konnten, dass die neue Methode tatsächlich funktioniert. Wir werden jetzt systematisch cfDNA sammeln und messen, um zu erkunden, was die Liquid Biopsy unter diesen Umständen tatsächlich zu leisten vermag, und wie sie dabei helfen kann, das Fortschreiten von Lungenkrebs unter Therapie noch besser zu verstehen.“ (DKFZ, red)
Riediger AL, Dietz S, Schirmer U et al.: Mutation analysis of circulating plasma DNA to determine response to EGFR tyrosine kinase inhibitor therapy of lung adenocarcinoma patients. Sci Rep. 2016 Sep 19;6:33505. DOI: 10.1038/srep33505.
Artikel teilen