Die Huntington-Erkrankung ist eine schwere, progressive Erkrankung des Zentralnervensystems. Sie bricht in der Regel im mittleren Lebensalter aus – also im Alter zwischen 20 und 50 Jahren. Uncharakteristische Frühsymptome sind zum Beispiel subtile Persönlichkeitsveränderungen und Konzentrationsverlust. Später, im manifesten Stadium, ist die Erkrankung durch eine Bewegungsstörung – im Fachjargon Chorea –, psychiatrische Symptome wie zum Beispiel Depressionen und Demenz charakterisiert. Innerhalb von etwa 10 bis 15 Jahren nach Ausbruch der Erkrankung versterben die Patienten. Die Huntington-Erkrankung ist eine Erbkrankheit mit einem 50-prozentigen Risiko für Patienten, die Erkrankung an ihre Kinder weiterzugeben. Nachkommen von Patienten sind somit nicht nur mit einem krank und kränker werdenden Elternteil konfrontiert, sondern auch mit ihrem eigenen Risiko, dieselbe Erkrankung auszuprägen.
Prädiktiv testen
Der Gendefekt, der zur Huntington-Erkrankung führt, ist seit den 90er Jahren bekannt. So wurde es möglich, Familienangehörige von Betroffenen prädiktiv zu testen. Trotz intensiver Forschung gibt es aber nach wie vor keine Therapie für diese schwere Erkrankung.
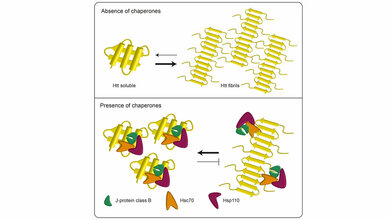
Wissenschaftler der Universitätsmedizin Mainz haben nun die Hypothese aufgestellt, dass die Huntington-Erkrankung nicht erst zum Zeitpunkt des Auftretens klinischer Symptome oder kurz davor das Gehirn angreift. „Wir haben überlegt, dass das aufgrund des Gendefekts veränderte Eiweiß wahrscheinlich bereits sehr lange vor der ersten Krankheitsmanifestation kleine Schäden im Gehirn verursacht und dass diese kleinen Schäden das neuronale Netzwerk subtil stören“, berichtet Univ.-Prof. Dr. Susann Schweiger, Direktorin des Instituts für Humangenetik und Sprecherin des Forschungszentrums Translationale Neurowissenschaften (FTN). „Wir haben weiter vermutet, dass die Behandlung dieser kleinen, sehr frühen Störungen nötig ist, um die Krankheit effektiv zu stoppen.“
Nutzung von hochauflösender 2-Photonen Mikroskopie
Diese Hypothese untersuchten die Wissenschaftler in Mäusen, die die Huntington Mutation tragen und im Laufe von etwa ein bis zwei Jahren eine Huntington-ähnliche Erkrankung entwickeln. Mit Hilfe von hochauflösender 2-Photonen Mikroskopie konnten sie im Gehirn der Mäuse – lange bevor diese Symptome zeigten – einzelne Neuronen identifizieren, die deutlich aktiver als der Rest der Zellen waren. Solche hyperaktiven Zellen wurden in gesunden Kontrolltieren nicht gefunden. „Weiterhin konnten wir zeigen, dass diese einzelnen hyperaktiven Zellen die Aktivität des gesamten Netzwerkes in Richtung Hyperaktivität verschieben“, erläutert Univ.-Prof. Dr. Albrecht Stroh vom Institut für Pathophysiologie.
Metformin mit neuroprotektiver Wirkung?
Aus ihren früheren Arbeiten war den Wissenschaftlern bekannt, dass das altbekannte Medikament Metformin, das gegen Typ II-Diabetes eingesetzt wird, auch neuroprotektive Wirkung haben kann. In ihrer aktuellen Arbeit konnten sie nun zeigen, dass durch Metformin-Gabe die frühen Veränderungen des neuronalen Netzwerks ebenso wie Verhaltensauffälligkeiten verschwinden. „Diese Ergebnisse bedeuten, dass Metformin, wenn es lange bevor die Krankheit ausbricht, verabreicht wird, den Krankheitsprozess im Tiermodell stoppen kann“, erklärt Susann Schweiger. „In künftigen Studien wollen wir nun untersuchen, ob sich mit den frühen, chronischen Metformingaben auch wirklich die später auftretenden Krankheitszeichen verhindern und Hirnnetzwerke stabilisieren lassen“, fügt Albrecht Stroh hinzu. Außerdem planen die Wissenschaftler eine proof-of-concept Studie mit Huntington-Patienten, die sich in einem frühen Krankheitsstadium befinden, um herauszufinden, ob die orale Gabe von Metformin auch im Menschen zur Reduktion von krankheitsverursachendem Eiweiß führt. „Wenn auch diese Untersuchungen erfolgsversprechend ausfallen, wäre der nächste Schritt zu untersuchen, ob durch Gabe von Metformin in sehr jungen Mutationsträgern die Huntington-Erkrankung tatsächlich aufgehalten werden kann“, zeigt Susann Schweiger die nächsten Schritte auf. „Dies wäre ein großer Erfolg, der aber noch einige Zeit dauern kann. So würde die proof-of-concept Studie etwa zwei Jahre in Anspruch nehmen. Die Anschlussstudie könnte dann in etwa drei bis fünf Jahren anlaufen.“
Eine ähnliche Erkenntnis zeigte die Studie von Florian A. Siebzehnrübl, Kerstin A. Raber, Yvonne K. Urbach, et al.: Early postnatal behavioral, cellular, and molecular changes in models of Huntington disease are reversible by HDAC inhibition. Auch diese Modelle zeigten, dass das Huntingtin-Gen bereits in der Kindheit die Gehirnentwicklung verändert und dass dies durch Medikamente, die die „Übersetzung“ des genetischen Codes in Eiweißmoleküle modulieren, aufzuhalten ist. (idw, red)
Isabelle Arnoux, Michael Willam, Nadine Griesche, et al.: Metformin reverses early cortical network dysfunction and behavior changes in Huntington's disease. eLife 2018;7:e38744, DOI: 10.7554/eLife.38744.
Artikel teilen