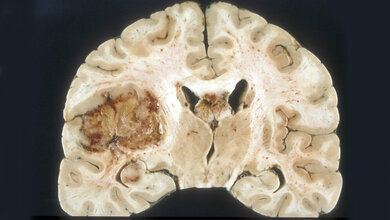
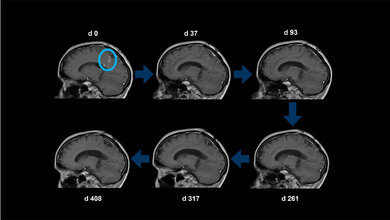
Die Diagnose Glioblastom gleicht noch immer einem Todesurteil. Die mittlere Überlebenszeit beträgt unverändert nur etwa 14 bis 15 Monate ab Diagnosestellung. Glioblastome sind die häufigsten und aggressivsten bösartigen Gehirntumore. Durch die operative Entfernung des Tumors und die zusätzliche Strahlen- und Chemotherapie lässt sich meist keine vollständige Heilung erreichen. Der Bedarf nach besseren Behandlungsmöglichkeiten ist entsprechend hoch. Eine neue Kombination aus einem Antikörper, der Krebszellen gezielt entdeckt, und einem Radionuklid weckt bei Reinhard Zeidler, Wissenschaftler bei Helmholtz Munich und am LMU Klinikum, Hoffnung: „Wir glauben, dass wir mit diesem Antikörper Glioblastome besser therapieren und die Lebenserwartung von Betroffenen verlängern können“.
Phase-I-Studie angelaufen
ITM Isotope Technologies Munich SE (ITM), ein radiopharmazeutisches Biotech-Unternehmen, Helmholtz München und die Kliniken für Neurochirurgie und Nuklearmedizin des Universitätsklinikums Münster gaben den Start einer klinischen Phase-I-Studie mit dem Arzneimittelkandidaten ITM-31 (ehemals LuCaFab) von ITM, einem neuartigen Kandidaten für die gezielte Radionuklidtherapie zur Behandlung von malignem Glioblastom bekannt. ITM-31 ist ein Carboanhydrase (CA) XII-spezifisches Antikörper-Fab-Fragment, das von Helmholtz München entwickelt wurde und mit dem medizinischen Radioisotop Lutetium-177 (n.c.a 177Lu, EndolucinBeta®) von ITM gekoppelt ist. Die Studie wird vom Universitätsklinikum Münster gefördert, an Kliniken in Münster, Essen, Köln, Würzburg durchgeführt und von ITM und Helmholtz München unterstützt. Die Patientenrekrutierung für die Studie läuft.
Wachstum zumindest verzögern
Der verheißungsvolle Antikörper* ist das Ergebnis aus vielen Jahren Grundlagenforschung. „Ohne ein großes Maß an Ausdauer hätten wir diesen Antikörper nicht bis hierher entwickeln können“, so Zeidler. „Er eignet sich deshalb so gut für die Krebstherapie, weil er Tumorzellen wesentlich präziser von gesunden Zellen unterscheiden kann als etwa eine Chemotherapie. Eine Behandlung verspricht deshalb deutlich weniger Nebenwirkungen.“ Zeidler betont: „Unser Ziel ist es, verbleibende Krebszellen, die mit der klassischen Behandlung nicht entfernt oder zerstört werden konnten, endgültig zu eliminieren.“ So soll das Medikament ein erneutes Wachstum des Tumors verhindern oder zumindest zeitlich verzögern.
*Der Antikörper bindet spezifisch an das Enzym Carboanhydrase XII, das im Gehirn ausschließlich auf Krebszellen vorkommt – vermutlich, weil es von großer Bedeutung für deren schnelles Wachstum ist. Gekoppelt an Lutetium-177, einen radioaktiven Strahler, hat der Antikörper einen doppelten Effekt: zum einen hemmt es das Enzym, zum anderen dirigiert er das Lutetium-177 spezifisch an die Tumorzellen, die durch die Standardtherapien nicht eliminiert werden konnten und die den Ursprung eines neuen Tumors bilden. Die beim radioaktiven Zerfall von Lutetium-177 freigesetzte Strahlung zerstört die Tumorzellen in der unmittelbaren Umgebung.
Quelle: idw/HZM
Artikel teilen