Im Jahr 2018 erkrankten in Deutschland laut Zentrum für Krebsregisterdaten rund 22.890 Personen am malignen Melanom der Haut, darunter etwa gleich viele Frauen wie Männer. Das mittlere Erkrankungsalter der Frauen ist mit 62 Jahren vergleichsweise niedrig. Männer erkranken im Mittel mit 68 Jahren. Hat ein malignes Melanom erst einmal gestreut und Metastasen in anderen Organen gebildet, sind die Heilungschancen geringer. Obwohl die Behandlung im fortgeschrittenen Stadium weiterhin eine Herausforderung darstellt, hat sich das Überleben der Patienten in den vergangenen zehn Jahren bedeutend verbessert. Dies ist insbesondere auf den Einsatz der Immuntherapie zurückzuführen: Hier wird das Immunsystem gegen den Tumor aktiviert, indem bestimmte Antikörper eingesetzt werden. Dennoch sprechen lediglich bis zu 40 Prozent der Patienten auf eine solche Immun-Checkpoint-Therapie an. Und auch nach erfolgreichem Ansprechen kann es zu einem erneuten Wachstum des Tumors kommen. Deshalb werden neue therapeutische Ansätze benötigt, um das metastasierende Melanom zu behandeln.
Einsatz von natürlichen Killerzellen?
Forscherinnen und Forscher der Universitätsmedizin Göttingen (UMG) in der Arbeitsgruppe von Prof. Dr. Ivan Bogeski, Professor für Molekulare Vegetative Physiologie am Institut für Herz-Kreislauf-Physiologie, haben dafür jetzt den Einsatz von natürlichen Killerzellen (NK-Zellen) untersucht. Die Forscher konnten anhand ihrer Ergebnisse erstmals neue NK-Zell-bezogene Biomarker nachweisen, die zu einer verbesserten und personalisierten Melanom-gerichteten Immuntherapie beitragen könnten. So könnte eine bessere Vorhersage getroffen werden, ob und wie gut eine Immuntherapie wirkt.
Vielversprechendes Werkzeug bei der Behandlung
Bisher wurden natürliche Killerzellen (NK-Zellen) bei der Entwicklung von Immuntherapien beim Melanom nicht berücksichtigt, dabei könnten diese therapeutische Vorteile für die Krebsbehandlung bieten. Natürliche Killer-Zellen haben zytotoxische Eigenschaften und können erkrankte Zellen abtöten. Im Gegensatz zu T-Zellen können sie ihre antitumorale Wirkung gegen einen Tumor richten, ohne vorher antigenspezifisch stimuliert werden zu müssen. Dies macht NK-Zellen zu einem vielversprechenden Werkzeug bei der Behandlung solider Tumoren. Allerdings sind NK-Zell-basierte Therapien bislang noch nicht verfügbar, obwohl aktuell einige vorklinische Studien laufen.
Entwicklung eines robusten Algorithmus
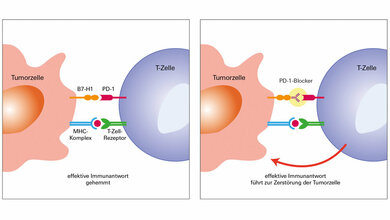
Die Immun-Checkpoint-Therapie verbessert die Überlebenserwartung bei Patientinnen und Patienten mit Melanomen und anderen Krebserkrankungen. Diese Therapien sind jedoch teuer und haben erhebliche Nebenwirkungen. Zudem liegen die Ansprechraten unter 40 Prozent. Bei der Immuntherapie wird das Immunsystem, insbesondere zytotoxische T-Zellen, gegen den Tumor aktiviert, indem Antikörper gegen CTLA4 (CTL-assoziiertes Protein-4) und PD (Programmed Cell Death Protein)-1/PD-L1 eingesetzt werden.
„Um Melanome besser behandeln zu können, wäre es von entscheidendem Vorteil, wenn sich vor der Behandlung der Tumorerkrankung vorhersagen ließe, ob der Tumor auf die Therapie anspricht“, sagt Dr. Sabrina Cappello, Erstautorin der Publikation. Zusammen mit ihren Kollegen hat sie zweidimensionale (2D) und dreidimensionale (3D) NK-Zell-basierte Zytotoxizitätsassays, Protein-Microarray-Screens, präklinische Tiermodelle und bioinformatische Analysen verwendet, um das zytotoxische Potenzial menschlicher NK-Zellen gegen Melanome zu erforschen. Darüber hinaus untersuchten die Forscher/-innen patientenindividuelle Datensätze und erstellten eine „Protein-Signatur“. Diese wurde verwendet, um einen robusten Algorithmus zu entwickeln, der die Sensitivität von Melanomen gegenüber Anti-PD-1-Checkpoint-Immuntherapien vorhersagt.
Microarray-Screenings und In-vitro-Zytotoxizitätsassays
„Die Ergebnisse der Studie könnten für Krebspatienten/-innen einen doppelten Vorteil bieten. Zum einen könnten die Untersuchungen angewendet werden, um das Ansprechen auf die bereits in der Klinik eingesetzte T-Zell-basierte Immuntherapien vorherzusagen. Zum anderen könnten Sie dazu beitragen, zukünftig NK-Zell-basierte Therapien zu entwickeln und zu optimieren“, sagt Prof. Dr. Ivan Bogeski, Professor für Molekulare Vegetative Physiologie am Institut für Herz-Kreislauf-Physiologie der Universitätsmedizin Göttingen (UMG). Hier könnten, so Prof. Bogeski, proteinbasierte Microarray-Screenings und In-vitro-Zytotoxizitätsassays als Grundlage für eine personalisierte Krebstherapie der Zukunft dienen. Darüber hinaus geht er davon aus, dass diese zum Beispiel schnelle Informationen über das zytotoxische Potenzial der Immunzellen des Patienten sowie über das Proteinabundanz-/Aktivitätsmuster liefern. Letztlich könnten diese Informationen zu einer zentralen Entscheidungshilfe für personalisierte Therapien werden, so Bogeski.
Quelle: idw/Unimedizin Göttingen
Artikel teilen