Wie bekämpfen GBP1-Proteine Bakterien?
Es ist ein hochkomplexer Prozess, wenn das menschliche Immunsystem fortwährend ein Heer an verschiedenartigen Eindringlingen abwehrt. Dazu sind unterschiedliche Truppen und vielfältige Waffensysteme notwendig. Während bereits Etliches über Abwehrzellen und ihre Strategien bekannt ist, liegen noch viele molekulare Details im Dunkeln. Ein Team um Professor Oliver Daumke, Arbeitsgruppenleiter am Max Delbrück Center, konnte nun den zentralen Aktivierungsmechanismus des Proteins GBP1 auflösen, das eine wesentliche Rolle bei der Bekämpfung bestimmter Bakterien spielt. Das Team berichtet darüber, wie sich das Protein aneinanderlagert, um die Eindringlinge einzukapseln und so zu eliminieren. „Die Erkenntnisse helfen, die menschliche Immunabwehr besser zu verstehen – und sie vielleicht in Zukunft gezielter zu stimulieren“, sagt Daumke.
Abwehr gegen Salmonellen und Shigellen
GBP1 steht für „Guanylat-bindendes Protein 1“. Es wird von Körperzellen nach einer Infektion gebildet und bindet spezifisch an GTP, ein Nukleotid und chemischer Energiespeicher innerhalb der Zellen. Dort steuert GBP1 die Abwehr gegen bakterielle Krankheitserreger wie Salmonellen und Shigellen, die teilweise schwere Durchfälle hervorrufen. GBP1 aktiviert gezielt die Immunabwehr. Außerdem bildet es eine Proteinhülle rund um die unerwünschten Eindringlinge, die deren Membran zerstört. So werden die Bakterien verwundbar und daran gehindert, sich zu vermehren. Obwohl diese Abwehrstrategie bekannt war, blieb unklar, wie sie im Detail abläuft und welcher zentrale molekulare Schalter im GBP1-Protein dafür verantwortlich ist.
Einsatz eines Kryo-Elektronenmikroskops
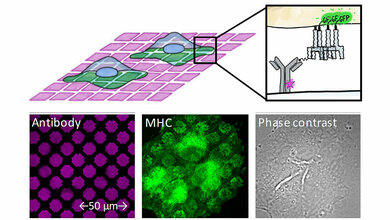
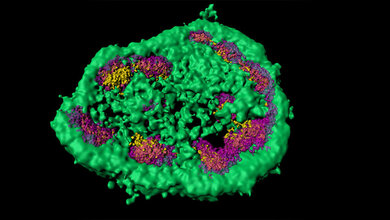
Mithilfe eines hochauflösenden Kryo-Elektronenmikroskops, mit dem sich die dreidimensionale Proteinstruktur darstellen lässt, untersuchte das Team diesen Prozess Schritt für Schritt: „GBP1 liegt zunächst als einzelner Baustein vor. Wird es aktiviert, klappt es ähnlich wie ein Schweizer Taschenmesser auf, es öffnet sich“, erklärt der Erstautor der Publikation Marius Weismehl, der als Doktorand in Daumkes Arbeitsgruppe forscht. „Tausende dieser aufgeklappten Proteine lagern sich dann zu Ringen zusammen, die sich wiederum zu Röhren aufstapeln“, fährt Weismehl fort. „Die Röhren heften sich schließlich an die Membran der Bakterien, wo sie sich neu formieren und wie ein Mantel um sie legen.“ Auf diese Weise eliminieren sie die Eindringlinge. Wie diese großen Proteinstrukturen im Detail aufgebaut sind, war zentrale Fragestellung ihrer Arbeit. „Unsere Mikroskopie-Daten zeigen eindrucksvoll, wie sich GBP1-Proteine ähnlich wie Stecknadeln an die Oberfläche von Membranen haften und sich über ihre Köpfe miteinander verbinden“, sagt Professor Misha Kudryashev. Diese neuen Erkenntnisse seien ein entscheidender Faktor, die mechanistische Funktionsweise von GBP1 zu entschlüsseln.
Gezielt bestimmte Stellen im Protein geändert
„Wir haben einen zentralen molekularen Hebel identifiziert, der für den ersten Schritt der Aktivierung ausschlaggebend ist“, sagt Weismehl. Dabei nutze das Protein die in GTP gespeicherte Energie, um diesen Hebel zu steuern und sich selbst zu aktivieren. Dieser Mechanismus erlaubt es dem Protein seine Form so zu ändern, dass es sich mit anderen Exemplaren verbinden kann und einen stabilen Proteinmantel um Bakterien bildet. Diese Erkenntnisse gewannen die Forscherinnen und Forscher, indem sie gezielt bestimmte Stellen im Protein änderten und so deren jeweilige Funktion aufdeckten.
Immunantwort im Krankheitsfall gezielt ankurbeln?
„Unsere Ergebnisse offenbarten erstmals den ausgeklügelten Aktivierungsmechanismus von GBP1, der zur Einkapselung von Krankheitserregern in eine antimikrobielle Proteinhülle führt“, fasst Daumke zusammen. In Zukunft ließe sich etwa erforschen, wie die GBP1-Proteinstrukturen mit weiteren Akteuren der Immunantwort interagieren und so nachgeschaltete Signalkaskaden auslösen, sagt Weismehl. Das Forschungsteam ist optimistisch, dass dieses grundlegende Wissen über das menschliche Abwehrsystem hilft, bakterielle Infektionskrankheiten besser zu verstehen und die Immunantwort im Krankheitsfall gezielt anzukurbeln.
Quelle: idw/mdc-berlin
Artikel teilen