Pseudomonas aeruginosa ist ein hartnäckiger Problemkeim, der viele Krankenhausinfektionen verursacht. Die Bakterien befallen Wunden, Harnwege oder verschleimte Lungen und sind die Haupttodesursache von Mukoviszidose-Patienten. Pseudomonas-Bakterien bilden Biofilme, die sie vor Antibiotika schützen. Ein Großteil der Erreger ist außerdem gegen viele Antibiotika resistent.
Resistenzmechanismen auf der Spur
Forscher des Helmholtz-Instituts für Pharmazeutische Forschung Saarland (HIPS) in Saarbrücken sind diesen Resistenzmechanismen auf der Spur. Bei der Sequenzierung von gefährlichen Pseudomonas-Stämmen aus klinischen Proben konnten nun die Verknüpfungsmoleküle in den Biofilmen, die Lektine, als biochemische Marker identifiziert werden. Diese Marker erlauben das schnellere Erkennen von gefährlichen Bakterienstämmen und den Einsatz einer zugeschnittenen Therapie für den Patienten.
Trotz der hohen Sequenzunterschiede, die zu dieser Markerfunktion führen, wurde gezeigt, dass die verschiedenen Lektin-Varianten vergleichbare Zuckerstrukturen binden. Somit kann mit Hilfe der Sequenz des Lektins eine Zuordnung zu den klinisch relevanten Pseudomonas-Stämmen erfolgen. Gleichzeitig kann ein und derselbe Wirkstoff zum Aufbrechen des Biofilms genutzt werden. Die Forschungsarbeiten wurden im Rahmen des Deutschen Zentrums für Infektionsforschung (DZIF) und in Kooperation mit dem Helmholtz-Zentrum für Infektionsforschung (HZI) in Braunschweig sowie Partnern in Grenoble (Frankreich) und San Diego (USA) durchgeführt und gerade erst veröffentlicht.
Bakterieller Schutzwall soll angegriffen werden
Die Behandlung von Infektionen mit P. aeruginosa ist sehr problematisch, denn durch die Bildung von Biofilmen ist der Keim sehr gut sowohl vor dem Immunsystem als auch vor Antibiotika geschützt. In einem Biofilm kann die Resistenz gegenüber Antibiotika um das 10 bis zu 1000-fache erhöht sein. Ziel der Forscher am Helmholtz-Institut für Pharmazeutische Forschung (HIPS) und am Helmholtz-Zentrum für Infektionsforschung (HZI) ist es deshalb, Substanzen zu entwickeln, die den bakteriellen Schutzwall angreifen können.
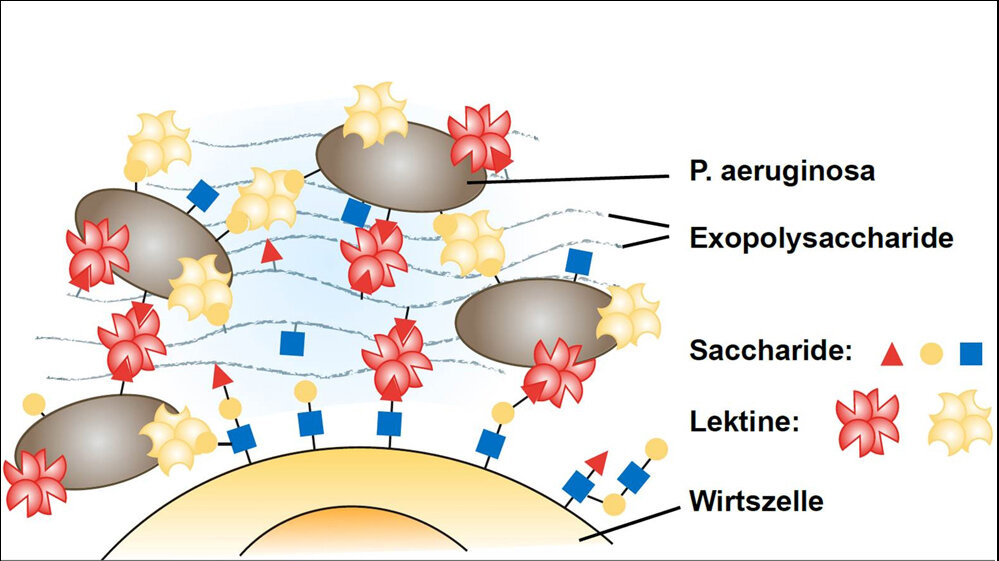
Im Fokus der Wissenschaftler stehen bestimmte Bausteine des Biofilms, die sogenannten Lektine. Diese Virulenzfaktoren spielen eine Rolle bei der Anheftung des Bakteriums an die Körperzellen und bei der Bildung eines Biofilms. „Die Lektine sind Proteinmoleküle, die die Bestandteile des Biofilms miteinander vernetzen können - sozusagen der Zement in der Mauer“, sagt Dr. Alexander Titz, Leiter der Nachwuchsgruppe „Chemische Biologie der Kohlenhydrate“ am HIPS in Saarbrücken. „Die Lektine können an mehreren Stellen Zuckermoleküle wie Mannose oder Galaktose, die sich auf den Oberflächen der Bakterien und den Wirtszellen befinden, binden und diese dann verknüpfen.“ Diese Zuckermoleküle wollen sich die Forscher nun zunutze machen und sie chemisch so manipulieren, dass sie zu Lektin-Inhibitoren werden. „Gelingt es uns, die Funktion der Lektine chemisch zu stören, verlieren die Bestandteile des Biofilms ihren Halt. Die Bakterien lösen sich aus der Lebensgemeinschaft heraus und werden für das Immunsystem und Antibiotika wieder sicht- und therapierbar“, sagt Titz. Dies ist ein aktueller Therapieansatz für biofilmbildende Pathogene und die damit zusammenhängenden chronischen Infektionen, der aufgrund seines Mechanismus Resistenzbildungen verhindern soll.
Stark variierende Sequenz des Lektins LecB
In einer Kooperation mit der HZI-Arbeitsgruppe „Molekulare Bakteriologie“ um Prof. Susanne Häußler wurde nun in einem nächsten Schritt die Erbinformation von 150 klinischen Isolaten von P. aeruginosa analysiert. Dabei wurden verschiedene Pseudomonas-Stämme, die sich in ihrer Biofilmbildung und ihrer Virulenz unterschieden, untersucht. Überraschendes Ergebnis war eine stark variierende Sequenz des Lektins LecB bei den Bakterienstämmen. Damit könnte dieses Lektin sehr gut als biochemischer Marker eingesetzt werden, um die unterschiedlich pathogenen Bakterienfamilien zu klassifizieren.
„Besonders auf Intensivstationen geht es um eine aussagekräftige Diagnostik, um zielgerichtet Therapien einleiten zu können. Zukünftig könnten nun die Lektine als Marker in der klinischen Diagnostik und in der Pharmazeutischen Industrie zum Erkennen von gefährlichen Pseudomonas-Stämmen herangezogen werden“, sagt Prof. Susanne Häußler.
Alternative für Antibiotika?
Die Forscher gingen noch einen Schritt weiter. Sie verglichen außerdem die Strukturen und Bindungseigenschaften der Lektine der gefährlichen und der weniger gefährlichen Stämme. „Obwohl sich die Lektin-Sequenzen beider Pseudomonas-Familien in der Sequenz unterscheiden, binden sie unerwarteterweise trotzdem gleiche Moleküle. Daher können wir nun spezielle Zuckermoleküle designen, die gegen ein breites Spektrum von gefährlichen Pseudomonas-Stämmen wirken und die Biofilmbildung blockieren“, erklärt Titz. Der Biofilm könnte auseinanderfallen und die Bakterien damit für antibiotische Medikamente angreifbar machen. Außerdem bestehe die Chance, dass diese Moleküle keine Resistenzen hervorrufen. Denn die Bakterien werden nicht getötet und einem Selektionsdruck ausgesetzt, wie das bei Antibiotika-Gabe der Fall ist. (idw, red)
The virulence factor LecB varies in clinical isolates: consequences for ligand binding and drug discovery: Roman Sommer, Stefanie Wagner, Annabelle Varrot, Corwin M. Nycholat, Ariane Khaledi, Susanne Häussler, James C. Paulson, Anne Imberty and Alexander Titz. Chem. Sci., 2016, Advance Article, DOI: 10.1039/C6SC00696E
Artikel teilen