Die Studie des Deutschen Krebskonsortium (DKTK) am OncoRay-Zentrum und der Klinik für Strahlentherapie am Universitätsklinikum Dresden zusammen mit Forschern des Helmholtz-Zentrums Dresden-Rossendorf (HZDR) bildet eine wesentliche Grundlage für die Entwicklung von Therapieverfahren, die stärker als bisher auf den individuellen Patienten zugeschnitten sind.
Oft Rezidive bei Glioblastomen
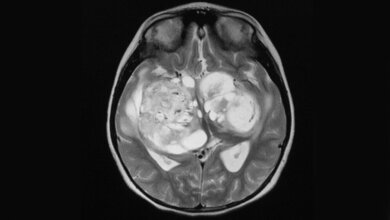
Patienten mit Glioblastom, einer besonders aggressiven Variante von Hirntumoren, entwickeln oft sogenannte Rezidive – das bedeutet, der Tumor kehrt trotz der Behandlung wieder. Um dies zu verhindern oder zumindest hinauszuzögern, werden die Patienten nach ihrer Tumoroperation intensiv mit einer Kombination aus Chemo- und Strahlentherapie nachbehandelt. Eine Gratwanderung: „Die Therapie erreicht nicht nur verbliebene Tumorzellen, sondern auch gesundes Gewebe“, erläutert Studienleiterin Mechthild Krause, Leiterin des OncoRay-Zentrums und der Klinik für Strahlentherapie am Universitätsklinikum Dresden. Darüber hinaus leitet Mechthild Krause das Institut für Radioonkologie am Helmholtz-Zentrum Dresden-Rossendorf (HZDR) und kooperiert als Standortsprecherin des DKTK eng mit dem Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg.
Patienten mit Kombination aus PET und MRT untersucht
„Für die PETra-Studie wurden unsere Patienten vor Beginn, während und nach Abschluss ihrer mehrere Monate dauernden Therapie mit einer Kombination aus PET und MRT untersucht“, erklärt Michael Baumann, Co-Leiter der Dresdner Studie und Vorstandsvorsitzender des DKFZ. Die Kombination aus Magnetresonanz- und Positronen-Emissions-Tomographie liefert den Medizinern deutlich mehr Informationen über die Gehirne ihrer Patienten. Die PET/MRT-Anlage am Universitätsklinikum Dresden entstand in enger Kooperation mit dem HZDR und war die erste dieser Art in Deutschland. Jetzt konnten die Forscher zeigen, dass sich der Therapieverlauf dank dieser Kombination deutlich besser vorhersagen lässt als bisher. „Unsere Langzeitdaten von insgesamt 89 Patienten bilden die Basis dafür, künftig etwa ein Therapieschema individuell möglichst passgenau, also so aggressiv wie nötig, aber so schonend wie möglich zu planen“, so Krause.
Manche Tumorareale durch die MRT gar nicht erkannt
Bisheriger Standard in der Bestrahlungsplanung von Patienten mit Glioblastomen ist die alleinige MRT-Untersuchung. „Dieses bildgebende Verfahren liefert uns Medizinern genaue Einblicke in die Hirnstrukturen der Betroffenen. Allerdings lässt sich nicht eindeutig erkennen, ob es sich bei bestimmten Auffälligkeiten um einen aktiven Tumor handelt oder Veränderungen durch die Therapie; zudem werden manche Tumorareale durch die MRT gar nicht erkannt“, schildert Studienärztin Annekatrin Seidlitz. Bettina Beuthien-Baumann, die die Studie am Universitätsklinikum Dresden nuklearmedizinisch betreut hat und inzwischen am DKFZ arbeitet, führt weiter aus: „Solche zusätzlichen Informationen liefert die PET, indem sie die Stoffwechselaktivität im Gewebe von außen sichtbar macht. Dazu haben wir den Patienten vor der Untersuchung einen speziellen Tracer, radioaktiv markiertes Methionin, verabreicht.“
Methionin als Tracer
Der Tracer reichert sich in den Krebszellen an und das Tumorgewebe wird dadurch auf dem Untersuchungsbild sichtbar. „Auf diese Weise lassen sich Patienten, bei denen der Tumor mit hoher Wahrscheinlichkeit zurückkehrt, schon vor Beginn der Radiochemotherapie identifizieren“, beschreibt Krause den Vorteil dieses Verfahrens für Therapieentscheidungen. „In Zukunft wäre bei den Betroffenen beispielsweise eine Behandlung mit einer erhöhten Strahlendosis denkbar. Gleichzeitig sehen wir aber jetzt auch Gruppen von Patienten mit dieser eigentlich als unheilbar geltenden Krankheit, die ihren Hirntumor mit sehr hoher Wahrscheinlichkeit viele Jahre überleben – für diese Patienten gilt es Therapieverfahren zu finden, die mit möglichst wenigen Nebenwirkungen einhergehen.“
Sensible Diagnostik dank kurzer Wege
Ermöglicht wurde die aktuelle Studie durch eine enge, fach- und einrichtungsübergreifende Zusammenarbeit – und eine aufwändige Logistik: „Das Methionin für die PET-Untersuchungen ist mit 11C-Kohlenstoffatomen markiert. Diese haben eine Halbwertszeit von lediglich 20 Minuten“, sagt Jörg Steinbach, Direktor des Instituts für Radiopharmazeutische Krebsforschung am HZDR. „Wir stellen daher das Methionin für jede einzelne Untersuchung separat her, prüfen nach standardisierten Verfahren eine Vielzahl von Qualitätsparametern und stellen es unmittelbar dem Behandlungsteam zur Verfügung.“
Weitere Studien stehen an
„Derzeit werden über 20 Prozent aller Strahlentherapie-Patienten der Klinik für Strahlentherapie am Universitätsklinikum in klinischen Studien behandelt“, sagt Krause. Entscheidend dazu beigetragen hat das radioonkologische Studienzentrum, das mithilfe der Finanzierung innerhalb des DKTK aufgebaut wurde. Auch für die individualisierte Therapie des Glioblastoms mittels PET/MRT-Diagnostik stehen zunächst noch weitere Studien an: „Derzeit überprüfen wir, wie genau sich anhand der Aktivitätsmuster in den PET-Bildern der Ort vorhersagen lässt, an dem ein Tumor wieder auftritt.“ Denn mit einer möglichst genauen Lokalisation ließe sich die Strahlentherapie noch weiter optimieren. (idw, red)
Mechthild Krause et al. (2018): Postoperative [11C]MET-PET predicts radiochemotherapy outcome in glioblastoma: a prospective trial, ESTRO 2018 Session CL12: Late-breaking abstracts and practice changing trials. Presentation number: OC-0594.
Artikel teilen