Die Parkinson-Krankheit betrifft Millionen Menschen weltweit. Bisher verfügbare Therapien behandeln nur Symptome, über die eigentlichen Ursachen der Erkrankung ist noch wenig bekannt. Die Erkrankung tritt zu einem sehr hohen Prozentsatz spontan auf; nur 5 bis 20 Prozent aller Fälle sind genetisch bedingt. Die vererbbare Form der Krankheit basiert auf genetischen Veränderungen in dem Gen, das für das Protein alpha-Synuklein (α-Synuklein) kodiert. Das Risiko an Parkinson zu erkranken, steigt grundsätzlich mit zunehmendem Alter, gipfelt allerdings zwischen dem 58. und 62. Lebensjahr. Inzwischen stehen auch einige Umweltfaktoren, wie z.B. Pestizide oder Metalle, im Verdacht, das Erkrankungsrisiko zu erhöhen.
Haben Metalle Einfluss?
Das Zusammenspiel von genetischen Mutationen des α-Synuklein-Proteins und der Auswirkung einer Exposition verschiedener Metalle haben nun Wissenschaftler des Göttinger Exzellenzclusters und des DFG-Forschungszentrums für Mikroskopie im Nanometerbereich und Molekularphysiologie des Gehirns (CNMPB) der Universitätsmedizin Göttingen (UMG) in Zusammenarbeit mit dem Max Planck Laboratory for Structural Biology, Chemistry and Molecular Biophysics of Rosario (MPLbioR, UNR-MPIbpC) und dem Instituto de Investigaciones para el Descubrimiento de Fármacos de Rosario (IIDEFAR, UNR-CONICET), Universidad Nacional de Rosario, Argentinien, sowie dem Institut für Neurowissenschaften und Medizin (INM-9) am Forschungszentrum Jülich genauer untersucht.
Kupfer ändert Aggregatbildung
Die Wissenschaftler entdeckten, dass Kupfer die Aggregatbildung des α-Synukleins signifikant verändert. Die neuen Forschungsergebnisse legen nahe, dass α-Synuklein Aggregate – anders als bisher vermutet – nicht die ursprüngliche Ursache der Neurotoxizität sind, die zum Absterben von Nervenzellen führt. Diese Erkenntnis eröffnet völlig neue Perspektiven für therapeutische Ansätze. Die Forschungsergebnisse wurden kürzlich veröffentlicht.
Forschungsergebnisse im Detail
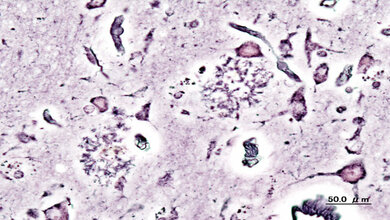
Morbus Parkinson ist eine langsam fortschreitende neurodegenerative Erkrankung. Die Krankheit gehört zu den sogenannten Synukleopathien. Charakteristisch ist eine außergewöhnliche Ansammlung von Aggregaten (Verklumpung) des Proteins alpha-Synuklein im Gehirn. Typisch sind motorische Symptome, wie Tremor, Muskelstarre, instabile Körperhaltung und Schwierigkeiten, Bewegungen zu initiieren. Ursache ist das Absterben von Dopamin-produzierenden Zellen im Gehirn. Eine mangelnde Versorgung mit dem Botenstoff führt zu einer unzureichenden Stimulation der motorischen Gehirnregionen.

Senior-Autor der Publikation:
Prof. Dr. Tiago F. Outeiro. Foto: CNMPB
Das Forscherteam unter der Leitung von Prof. Dr. Tiago F. Outeiro, Direktor der Abteilung Neurodegeneration und Restaurationsforschung an der Universitätsmedizin Göttingen (UMG), hat herausgefunden, auf welche Weise die einzigartige Kombination von Kupferionen und eine ganz bestimmte Mutation (H50Q) im kodierenden Gen für α-Synuklein-Protein die Verklumpungswahrscheinlichkeit des Proteins verändert.
Interaktion zwischen H50Q und Kupferionen
Kupfer ist ein Metall, das mit neurodegenerativen Prozessen in Verbindung gebracht wird, die zum Funktionsverlust oder Untergang von Nervenzellen führen. H50Q steht für eine krankheitserzeugende Mutation, die bei einigen Parkinson-Patienten nachgewiesen wurde. Durch die Integration von strukturellen Daten und Simulationen konnten die Forscher auf molekularer Ebene eine Erklärung für die Interaktion zwischen H50Q und Kupferionen gewinnen.
„Nur durch die Kombination verschiedener Expertisen und interdisziplinäre Kollaborationen waren wir in der Lage, entscheidende Erkenntnisse über Krankheitsmechanismen zu gewinnen“, sagt Prof. Dr. Outeiro, Senior-Autor der Publikation. Die strukturellen Daten lieferte das „Max Planck Laboratory for Structural Biology, Chemistry and Molecular Biophysics of Rosario“ im Forschungszentrum der Universidad Nacional de Rosario, Argentinien, unter der Leitung von Prof. Dr. Claudio Fernandez. Die nötigen Simulationen wurden am Institut für Neurowissenschaften und Medizin (INM-9) am Forschungszentrum Jülich von Prof. Dr. Paolo Carloni mit seinen Mitarbeitern Juniorprofessorin Dr. Giulia Rossetti und Enrique Abad durchgeführt. „Die Verbindung von Zellstudien mit unseren biophysikalischen Methoden zeigt, wie wichtig die Untersuchung gemeinsamer Effekte multipler Faktoren der Proteinbiologie tatsächlich ist“, sagt Prof. Dr. Claudio Fernandez.
Kombination quanten- und molekularmechanischer Simulationstechniken
„Die Kombination quanten- und molekularmechanischer Simulationstechniken (QM/MM), sind die Methoden der Wahl, um komplexe Interaktionen und spektroskopische Eigenschaften von übergangsmetallenbasierten Proteinen wie Kupfer(II)-ionen gebunden an α-Synuklein, vorherzusagen“, sagt Jun.-Prof. Dr. Giulia Rossetti. Der Zugang zur Supercomputinginfrastruktur in Jülich machte auch hier den entscheidenden Unterschied: Die Ergebnisse, die durch unsere QM/MM Studien erhalten wurden, benötigten beinahe ein Dutzend Millionen core hours auf JURECA.“
Prof. Dr. Tiago F. Outeiro ist Leiter der Abteilung Neurodegeneration und Restaurationsforschung an der Universitätsmedizin Göttingen. Zudem ist er Mitglied des Göttingen Exzellenzclusters und DFG-Forschungszentrums für Mikroskopie im Nanometerbereich und Molekularphysiologie des Gehirns (CNMPB). Seine Forschungsarbeit konzentriert sich auf die Entschlüsselung der grundlegenden molekularen Mechanismen, die bei neurodegenerativen Prozessen in Krankheiten, wie der Parkinson, Huntington oder der Alzheimer Erkrankung eine Rolle spielen. (idw, red)
Literatur:
Villar-Piqué A, Lopes da Fonseca T, Sant’Anna R et al. (2016): Environmental and genetic factors support the dissociation between α-synuclein aggregation and toxicity. PNAS, 113(42): E6506-6515.
Artikel teilen